患者さんに対する臨床研究について
・医学研究や臨床研究等の協力者となることを、拒むことができます。
・研究で使用する情報は厳重に管理され、研究目的のみで利用されます。
・検査結果や診療情報は統計として処理・解析されるため、個人を特定できることはありません。
臨床研究
- データバンクへの情報提供についてのお知らせ 掲載期日 2032年12月31日
- 女性患者における造血細胞移植後の妊娠の詳細調査 掲載期日 2027年12月31日
- ヒルシュスプルング病類縁疾患における中央病理診断の確立と臨床・病理学的解析 掲載期日 2030年3月31日
- 脳動脈瘤の安定性と脂質及び脂肪酸の関連性 掲載期日 2027年3月31日
- 脳動脈瘤塞栓術におけるバルーン付きガイディングカテーテル使用と術中破裂後の転帰との関連 掲載期日 2027年12月31日
- 乳癌に対する腋窩リンパ節評価省略が術後補助療法選択に与える影響に関する後ろ向き観察研究 掲載期日 2027年12月31日
- 高齢者の消化管穿孔および急性腸管虚血における術後ADL低下リスク因子の検討:多機関共同コホート研究 掲載期日 2028年3月末
- 脳外科病棟における誤嚥性肺炎予防の発症軽減に向けた取り組み、手順書の導入前後での比較検討 掲載期日 2026年12月末
- 術前治療後に切除した膵癌症例の予後に関する多施設共同研究 掲載期日 2028年3月31日
- タキサン系抗がん薬治療患者における非薬物的介入と末梢神経障害の関連―後方視的観察 研究― 掲載期日 2026年12月31日
- 間質性肺疾患の既往があるHER2陽性、低発現の進行再発乳癌患者におけるT-DXd投与の後ろ向きコホート研究 掲載期日 2027年3月末
- 乳房再建術後乳癌患者における乳房全切除術後放射線療法の有効性と安全性に関する観察研究(多機関共同研究)-日本乳房オンコプラスティックサージャリー学会班研究- 掲載期日 2027年3月末
- 乳癌の手術を目標とした術前化学療法と、超音波検査による効果判定について 掲載期日 2026年6月末
- 乳がん手術による肩関節拘縮を予防・改善し、安全な周術期治療とスムーズな完遂を支える患 者支援体制の強化 掲載期日 2026年4月末
- 乳腺診療における多機関臨床情報データベースを用いたリアルワールドエビデンスの創生 掲載期日 2027年3月末
- 若年者自然気胸に対し切除されたブラの病理形態学的検討 掲載期日 2026年3月31日
- 肺癌コンパクトパネル全国リアルワールドデータ後ろ向き集積研究 掲載期日 2028年3月31日
- 「気管支鏡検査時の鎮静におけるミダゾラム,フェンタニル併用の有用性と安全性の後方視的検討」の研究事業への、御協力をお願いするための説明文 掲載期日 未定
- 切除不能肝細胞癌に対する全身薬物療法の安全性と有効性に関するデータベース構築研究 掲載期日 2034年12月末まで
- 80歳以上の切除可能膵癌に対する術前補助療法の治療成績~多機関前向き観察研究 掲載期日 2028年12月末まで
- AYA世代と非AYA世代の乳房再建率・術式選択の比較に関する単施設後方視的観察研究 掲載期日 2026年11月1日まで
- 市販薬、食品によるカフェイン中毒に関する後方視的研究 掲載期日 2027年3月末まで
- 関節リウマチと腸内細菌由来脂質代謝物、腸内細菌叢のプロファイルの違いに着目したデータベース研究 掲載期日 2027年3月末まで
- 消化器内視鏡に関連する疾患、治療手技データベース構築(多機関共同 前向き観察研究) 掲載期日 2028年12月末まで
- 肺癌に対する免疫チェックポイント阻害剤の治療実態と有効性・安全性の検討 掲載期日 2035年3月末まで
- 多施設共同骨髄系腫瘍レジストリ研究 (MYKURE:Myeloid Malignancy Kyoto University Registry)」 についてのご説明 掲載期日 2030年3月末
- 研究課題 多分野合議による間質性肺炎診断に対する多施設共同前向き観察研 究に関する情報公開 掲載期日 2036年7月末
- 脳神経外科の外来診療あるいは入院診療を受けられた患者さんへ 掲載期日 2030年12月末
- 初発のFLT3変異陽性急性骨髄性白血病(AML)に対するキザルチニブ併用療法後にギルテリチニブを投与された再発・難治性AML患者の臨床転帰を評価する後ろ向き観察研究 掲載期日 2026年12月末
- 両側乳房再建術の術式選択理由と術後満足度に関する検討 掲載期日 2026年12月末
- 「転倒防止におけるアセスメント精度と標準対策遵守の実態分析」 掲載期日 2027年3月末
- 皮下植え込み型中心静脈ポート感染に関する現状調査と課題 掲載期日 2026年3月
- 多職種で開催した医療従事者体験は、高校生の進路・職業選択に影響を与えるか 掲載期日 2026年6月
- クロピドグレルとプラスグレルのPRU(P2Y12 reaction unit)値の比較検討
- 臨床研究「中規模病院における多職種連携によるAST活動の工夫とその効果」について
- BRCA遺伝学的検査に関するデータベースの作成 掲載期日 2028年12月末
- 肺非結核性抗酸菌症の治療状況の検証および疾患進行に寄与する因子の検討
- 気管支肺胞洗浄液細胞分画解析における自動分析装置と目視法の比較検討
- JBCRG-ABCD project(進行・再発乳がんデータベースプロジェクト)へのご協力のお願い
- CT画像報告書の説明漏れを防ぐための組織的な取組みの検討
- 当院におけるがん遺伝子パネル検査を受ける患者の現状と看護の課題
- 術前主膵管径3mm以下で柔らかい膵実質を持つ症例における膵液瘻リスク因子の同定:DAIMONJI-Study事後解析
- 免疫チェックポイント阻害薬投与終了後に新規発症する遅発性甲状腺機能障害についての後方視的研究
- 造血器疾患における遺伝子異常の網羅的解析研究 掲載期日 2030年3月末
- 血液中miRNA測定による消化器癌の診断法確立に向けた研究
- 抗エミシズマブ抗体と血漿中エミシズマブ濃度及び各種凝固検査値との関連性を評価する多機関共同臨床研究 掲載期日 2028年4月末
- 肺高血圧症発症や増悪のリスク因子を同定するための後方視的検討
- 当院で入院中に嚥下調整食の提供を受けられた患者様・ご家族様へ研究へのご協力のお願い
- 慢性移植片対宿主病に対する体外フォトフェレーシス治療の有効性に関する検討
- 血液培養よりクロストリジウムが分離されたの患者さんおよびご家族へ 【過去の治療データを調査研究への使用のお願い】
- 「ICG蛍光法センチネルリンパ節生検施行後の予後を調査する観察研究」について 掲載期日 2026年12月31日
- 「乳癌/卵巣癌既往があるAML・ALL・MDS患者における同種移植成績及び移植後のHBOC関連癌再発/発症リスクに関する検討」について
- 「FCM(フローサイトメーター)検査と臨床検査所見の症例検討」について
- 「神鋼記念病院における下部消化管出血の特徴及び治療成績の検討」について
- 「ブリナツモマブ治療後に同種造血幹細胞移植を施行した再発・難治性B 細胞性急性リンパ性白血病の臨床アウトカム」について
- 「当院で生じた免疫チェクポイント阻害剤による消化器有害事象の特徴及び対応についての検討」について
- 「筋炎特異自己抗体、筋炎関連自己抗体を有する間質性肺炎の後方視的観察研究」について
- 「神鋼記念病院におけるロボット支援腹腔鏡下腎部分切除術(RAPN)の治療成績、播種再発を来した症例の検討」について
- 「術前治療後に切除し病理学的完全奏効(pCR)であった膵癌症例における臨床病理学的意義の検討」について
- 「80歳以上の高齢鼠径ヘルニア患者に対する至適手術治療の検討」について
- 「閉経前ホルモン受容体陽性乳癌の術後内分泌療法に関した後方視的研究」について
- 「バンコマイシンの1点採血と2点採血のAUCの比較」について
- 「当院のHoLEPの術式変更と術後尿失禁の検討」について
- 「原発性アルドステロン症における腹腔鏡下副腎摘除術後の高血圧治療成績についての検討」について
- 「呼吸器疾患患者における将来の肺高血圧症発症の予測手法を確立するための後方視的検討」について
- 「関節リウマチ患者における生物学的製剤投与前後の抗核抗体の変化と抗薬物抗体との関連性の検討」について
- 「HAM患者レジストリ『HAMねっと』を活用した病態解明および治療法・予防法の開発に関する研究」について
- 「進行性の線維化を有する間質性肺炎患者における抗線維化薬の減量・中止に関わる因子の探索及び中止・減量が予後に与える影響の後方視的調査」について
- 「全国放射線治療症例に基づく放射線治療の実態調査および質評価」について
- 「アベマシクリブ(ベージニオ®)投与患者における有害事象発現のリスク因子に関する研究」について
- 「造影マンモグラフィの乳癌画像診断への適用に関する研究」について
- 「JBCRG-ABCD project『進行・再発乳癌データベースプロジェクト(Advanced Breast Cancer Database Project)』」について 掲載期日 2029年12月31日
- 「3群肺高血圧症患者レジストリー(JAPHR3群)と連携した呼吸器疾患の胸部CTの定量評価と臨床病態解析に基づいた予後予測モデルの構築」について 掲載期日 2029年3月31日
- 「EGFR遺伝子L858R変異陽性進行再発非扁平上皮非小細胞肺癌に対するRamucirumab + Erlotinibの有効性及び安全性を評価する多機関共同・後方視的観察研究(REAL-SPEED)」について
- 「一般病院からがんゲノム医療連携病院へ依頼する包括的がんプロファイル検査の現状と問題点」について
- 「過敏性肺炎の全国疫学調査」について
- 「当院におけるロボット支援腹腔鏡下前立腺全摘術における術後の腸閉塞およびイレウスの発生率と危険因子についての検討」について
- 「メタボローム解析によるピロリン酸カルシウム結晶沈着症の診断バイオマーカーの同定」の研究 掲載期日 2027年3月末
- 「SARS―CoV2ワクチン接種後に生じたリウマチ性疾患についての全国調査」について
- 「椎骨動脈スタンプ症候群に対する血管内治療」について
- 「特発性間質性肺炎における赤血球容積分布幅と肺高血圧症の関連についての単施設後方視的コホート研究」について
- 京都造血幹細胞移植グループの造血幹細胞移植データを用いた移植成績の解析 掲載期日 2030年3月末
- 「再発・難治性FLT3変異陽性急性骨髄性白血病の患者さんに対するギルテリチニブの安全性・有効性の検討」について
- 「慢性咳嗽・喘息・COPD患者の治療やコントロール状況の調査および各種臨床指標と将来のリスクの関連の検討」について
- 「特発性好酸球増加症候群において多施設共同研究の既存試料と既存資料を利用し病態関連バイオマーカーを探索する観察研究」について
- 「日本病理剖検輯報に基づく全身性アミロイドーシス各病型頻度の疫学調査」ご協力へのお願い
- 「間質性肺炎に対する抗線維化薬ニンテダニブ・ピルフェニドン投与が肺血行動態に与える影響評価」について
- 「コロナウィルス肺炎(CoVP)とインフルエンザウィルス肺炎(InVP)、非ウィルス性市中肺炎(nVCAP)の臨床像に関する多施設共同研究のお知らせ」について
- 「COVID-19 に関するレジストリ研究」について
- 「前立腺癌患者におけるアビラテロン併用アンドロゲン遮断療法が骨量に与える影響の観察研究」について
- 「本邦リアルワールドでの重症喘息における生物学的製剤の使用実態および効果に寄与する因子の検討」について
- 「全国胆道癌の後方視的観察研究」について
- 「日本整形外科学会症例レジストリー(JOANR)構築に関する研究」について
- 「乳がん微小環境形成に関わる分子生物学的機序の生体資料を用いた探索研究」について
- 「肺高血圧症患者の四肢骨格筋機能がQOL(生活の質)に与える影響評価」について
- 神鋼記念病院脳神経外科にて神経系疾患で入院された方およびそのご家族の方へ
- 乳がん微小環境形成に関わる分子生物学的機序の生体資料を用いた探索研究
- 「乳房良悪性病変のgadobutrol* 造影 MRI 画像における画像的特徴に関する検討」について
肺非結核性抗酸菌症の治療状況の検証および疾患進行に寄与する因子の検討
本件は「オプトアウト」すなわち,同意不要であった既存データを用いた研究において、「自分の データは使わないでほしい」という、患者さんの拒否の機会を確保するため、研究の公開をホームページ上で行っているものです。 今回の研究に該当されることが予想され、「自分のデータは使わないでほしい」と希望される方はご本人・ご家族より当院に手紙、メール、お電話もしくはファックスなどにてその旨ご連絡ください。
神鋼記念病院呼吸器内科に通院中の肺非結核性抗酸菌症の患者さんへ
実施する臨床研究
肺非結核性抗酸菌症の治療状況の検証および疾患進行に寄与する因子に関する臨床研究を実施しております。この研究は「観察研究」と呼ばれるもので、 通常の診療で得られた記録をまとめることによって行います。以下の点をご理解いただき、ご協力いただきますようお願い申し上げます。
この研究の意義、目的、および方法
近年、肺非結核性抗酸菌症(以下、NTM症)が増加の一途をたどっています。NTM症は無治療でも長期間悪化のない症例から、様々な治療にもかかわらず進行していく症例まで経過は様々です。悪化に関連する因子として年齢、菌種およびその治療、画像病型、栄養状態などに加え全身や肺の基礎疾患などが報告されています。炎症性疾患に対する生物学的製剤の普及など基礎疾患およびそれぞれの治療は変化しており、NTM症の患者さんの背景因子や臨床経過も変化していることが予想されます。本研究ではNTM症患者の背景因子を調査し、治療状況を検証するとともに疾患の進行に関連する因子を検討します。日常臨床で行われる問診や採血データ、喀痰検査、画像(レントゲンやCT)などを用いて調査し、将来のNTM症の管理に役立てることを目的とします。
この研究による医学上の貢献と予測
NTM症の進行を予測する因子の検討をとおして最適な管理方法を検討します。
研究の対象者
2015年4月1日以降にNTMのために当科に通院歴のある患者さんを対象とします。
この研究による患者さんの不利益および危険性
患者さんの診療情報を分析する研究であり、プライバシーも厳重に保護されますので、患者さんに不利益や危険性はありません。
費用や追加の検査
通常の保険診療による画像診断情報と臨床情報の収集と分析ですので、患者さんに余分な費用を負担してもらうことはありません。また、検査方法の変更や追加検査もありません。
個人情報の保護
この研究で得た情報は厳重に管理され、学術目的のみで利用されます。 研究結果は主として統計として処理・解析され発表されるため、個人を特定できることはありません。研究結果の発表に際して、一部の患者さんの臨床情報が参考所見として呈示される可能性がありますが、匿名化されていますので、個人を特定できることはありません。 本研究参加者以外の第三者に流出することもありません。以上のように、患者さんのプライバシーは厳重に保護されますのでご安心ください。
ご協力の拒否について
この研究にご自分のデータが使用されることを拒否される場合は、担当医もしくは下記の問い合わせ先に連絡下さい。 たとえ、協力を拒否されても、今後の診療の不利益になることはありません。しかし、拒否のお申し出のあった時点で、 既に研究結果が論文などで公表されていた場合には、 研究結果を破棄できないことがあります。 この場合でも個人が特定されることはありませんので個人情報は保護されます。
研究責任者
神鋼記念病院 呼吸器内科 大塚 浩二郎
当院における連絡先
神鋼記念病院 呼吸器内科 大塚 浩二郎
〒651-0072 神戸市中央区脇浜町1丁目4-47
TEL:078-261-6711 ・ FAX:078-261-6931
気管支肺胞洗浄液細胞分画解析における自動分析装置と目視法の比較検討
本件は「オプトアウト」すなわち、同意不要であった既存データを用いた研究において、「自分のデータは使わないでほしい」という、患者さんの拒否の機会を確保するため、研究の公開をホームページ上で行っているものです。 今回の研究に該当されることが予想され、「自分のデータは使わないでほしい」と希望される方はご本人・ご家族より当院に手紙、メール、お電話もしくはファックスなどにてその旨ご連絡ください。
神鋼記念病院で気管支肺胞洗浄を行われた患者さんへ。
実施する臨床研究
該当する患者さんの診療経過について調査研究を実施しております。この研究は「観察研究」と呼ばれるもので、 通常の診療で得られた記録をまとめることによって行います。以下の点をご理解いただき、ご協力いただきますようお願い申し上げます。
この研究の意義、目的、および方法
気管支肺胞洗浄(BAL)は、肺の奥から液体の検体を採取し、それを調べることで病気の診断に役立てる検査です。検査では、口や鼻から細いカメラ(気管支鏡)を肺の中まで入れ、生理食塩水を肺に流し込んでから回収し、その液体を調べます。肺の深い部分にある分泌物や細胞を取り出して調べることで、さまざまな肺の病気の診断に役立ちます。
この検査は、間質性肺疾患(肺の組織に炎症や傷が起きる病気)や肺感染症、薬の副作用による肺炎、アレルギーに似た反応による肺炎(過敏性肺炎)、肺の中の出血、免疫力が落ちたときに起きる感染症など、さまざまな病気を調べるときに使われます。BALによって、肺の中にどのような細胞や菌がいるのかがわかり、病気の診断に直接つながることがあります。
肺の検査には、他にも肺の組織を一部採る「肺生検」などの方法がありますが、これらに比べるとBALは体への負担が比較的少ない方法です。画像検査、特に高分解能CT(HRCT)で多くの情報を得られるようになってきましたが、画像だけでは診断が難しいケースもあり、そのようなときにBALの情報が参考になります。
特に過敏性肺炎では、BALで採取した液の中に含まれるリンパ球という種類の白血球が増えていることが診断の手がかりとなります。この考え方は、国内外の専門的なガイドラインにも取り入れられています。
検査の結果を正確に得るためには、採取の方法や保存の仕方、検査の手順がとても重要です。これまで、液体の中の細胞の種類を人の目で確認する「目視法」が一般的でしたが、最近では自動で細胞を分類・測定できる分析装置も使われ始めています。当院では2023年2月から「XNシリーズ」という自動分析装置を導入し、目視法と併用してBALの検体を分析しています。
この分析装置は、特殊な方法で細胞を染めてからレーザーを当て、その反応から細胞の種類や数を判断するしくみになっています。数値だけでなく、図として結果が表示されるのも特徴です。ただし、特殊な細胞(がん細胞など)の見分けは難しいことがあり、検体の状態や細胞の数が少ない場合には、結果が目視法と異なることがあります。そのため、必要に応じて目視法での再確認を行うことがあります。
本研究では、自動分析装置と目視法で得られた結果に違いがあるかどうか、またどのような条件でその違いが生じるのかを調べています。これにより、BALの結果をより正確に判断し、診断や治療に活かすことを目的としています。
この研究による医学上の貢献と予測
日常臨床で得られる情報を通して、気管支肺胞洗浄を受けられる患者さんに、より適切な診療を届けられる方法を検討します。
この研究による患者さんの不利益および危険性
患者さんの診療情報を分析する研究であり、プライバシーも厳重に保護されますので、患者さんに不利益や危険性はありません。
費用や追加の検査
通常の保険診療による画像診断情報と臨床情報の収集と分析ですので、患者さんに余分な費用を負担してもらうことはありません。また、検査方法の変更や追加検査もありません。
個人情報の保護
この研究で得た情報は厳重に管理され、学術目的のみで利用されます。 研究結果は主として統計として処理・解析され発表されるため、個人を特定できることはありません。研究結果の発表に際して、一部の患者さんの臨床情報が参考所見として呈示される可能性がありますが、匿名化されていますので、個人を特定できることはありません。 本研究参加者以外の第三者に流出することもありません。以上のように、患者さんのプライバシーは厳重に保護されますのでご安心ください。
ご協力の拒否について
この研究にご自分のデータが使用されることを拒否される場合は、担当医もしくは下記の問い合わせ先に連絡下さい。 たとえ、協力を拒否されても、今後の診療の不利益になることはありません。しかし、拒否のお申し出のあった時点で、 既に研究結果が論文などで公表されていた場合には、 研究結果を破棄できないことがあります。 この場合でも個人が特定されることはありませんので個人情報は保護されます。
研究責任者
神鋼記念病院 呼吸器内科 門田 和也
当院における連絡先
神鋼記念病院 呼吸器内科 門田 和也
〒651-0072 神戸市中央区脇浜町1丁目4-47
TEL:078-261-6711 ・ FAX:078-261-6931
JBCRG-ABCD project(進行・再発乳がんデータベースプロジェクト)へのご協力のお願い
これからJBCRG-ABCD project(進行・再発乳がんデータベースプロジェクト)について説明します。このプロジェクトに参加されるかどうか、あなたの自由意思で決めてください。ご不明な点や心配なことがあれば遠慮なくご質問ください。なお、ご返事は今日でなくてもかまいません。この説明文書をお持ち帰りになり、後日お返事くださっても結構です。研究の内容を十分ご理解のうえ、あなたの同意が得られれば、ご協力いただきたく存じます。
なお、このプロジェクトの当病院での実施にあたっては、東海大学医学部臨床研究審査委員会でこの研究の内容について科学的、倫理的な観点から審議・承認され、当院の病院長の実施許可を得ています。
また、このプロジェクトは、一般社団法人JBCRG(Japan Breast Cancer Research Group、以下JBCRGという。)がおこない、JBCRGに所属する日本各地の乳がん専門医が所属する施設が、乳がんの状況や治療に関する情報を、以下の目的で使用します(JBCRGは、日本国内やほかの国および地域と連携をしながら、臨床研究を遂行することを主な目的として設立された非営利の法人です)。
1.本データベースプロジェクトの意義・目的
あなたの病気の診断や診療の際に得られた臨床情報や画像・血液検査のデータなどは、将来、同じ疾患の方の診断や治療の発展につながる可能性のある大切な情報であり、医療の進歩のために必要なものです。また、遺伝子解析技術の著しい進歩により、病気の原因・診断・治療法の選択に活用できるゲノム・遺伝子情報が増えてきました。臨床情報と遺伝子検査結果の情報を用いて、遺伝子情報に基づいた適切な治療を行うための研究が重要となっています。
データベースプロジェクトの目的と臨床情報の提供範囲
本プロジェクトでは、JBCRGに所属する国内の主要な乳がん治療を専門とする病院と協力して、第3者からは個人を同定できないように加工された臨床情報をデータベースに登録、保管します。このデータベースプロジェクトの目的は、進行・再発乳がんに対する最適な治療法を明らかにするためなどの臨床研究を行う基盤を作ることです。
このデータベース内の臨床情報は、以下のように利用されます。
1.国内の研究者に臨床情報を提供し、進行・再発乳がんに対する最適な治療法を明らかにするためなどの臨床研究を行います。
2.多施設における治療施行状況と治療効果等の臨床情報を参加施設の医師に提供し、最適な治療方法をフィードバックする体制を構築します。
3.進行・再発乳がんの臨床試験とデータベース内の情報を結合し、その情報を長期的に利用できるように整備・保管していきます。
4.開発中の新しい薬の効果を明らかにするための治験や、新しい治療法の有用性を明らかにする臨床試験に関する情報を、医師に提供する予定です。
5.治療薬・検査測定機器が適切に使用されているかなどを検討することを目的に、国内の医療関係機関(民間企業等)に、治療薬や検査に関する臨床情報の集計データ等を提供します。
2.プロジェクトへの自由意思による同意と同意撤回
今回のプロジェクト参加のお願いに対して同意するか否かは、あなたの自由です。また、同意した後で同意の撤回やデータの削除を求めることも可能です。担当医あるいは問い合わせ窓口へお申し出ください。同意されなかったとしても、今後のあなたの診療にはまったく影響はありません。参加後も、参加を中止したいと思った場合は、いつでも担当医師に申し出ることが可能です。参加の中止をご要望の場合、この研究でデータベースに保管されるあなたの臨床情報の取扱いについて、同意撤回書でお知らせください。同意を撤回されても、あなたの不利益になることはありません。
3.予期される利益と不利益
既にあなたが受けられた診療の情報を登録してデータが集積されるため、あなたに新たに負担が生じることは有りません。また、あなたがこの研究に参加することにより、謝礼等の提供はないことを予めご了承ください。
この研究により、今のあなたの診療に役立つ情報(利益)を得ることはできないのですが、今後の進行・再発乳がん患者さんにとっては有用な情報になっていくことが期待されます。
一方、不利益としては、情報の漏えいが考えられます。情報を登録する際には、個人を識別できる情報は削除して提出しますので、個人情報が漏えいすることは通常ありませんが、リスクが全くないと言い切れるものではありません。個人情報保護については、以下に示す対応をとっています。
4.個人情報の保護について
収集する臨床情報
このデータベースには、お名前、住所、電話番号等の個人を同定できる情報は収集されることはありません。あなたの性別、生年月日(※ご施設により日の提供がむずかしく、任意の日を設定される場合は「日」を削除してください)、病気の状態やがんの性質、使用した薬剤名、治療効果、治療終了理由、施行された手術や放射線療法に関する情報や遺伝子変異などの検査結果等が保管されます。
データベースにこれらの臨床情報を保管する際、研究用番号とそれぞれの病院の患者カルテ番号によって個人を識別します。外部の研究者や医療機関にはそれらの番号は提供しませんので、あなた個人を特定することはできません。
データベースにこれらの臨床情報を保管する際、研究用番号をつけて個人を識別します。個人と研究用番号を照合する対応表は、あなたが受診している施設のみで保有されるので、外部の研究者や医療機関があなた個人を特定することはできません。
情報の管理方法
米国ヴァンダービルト大学が開発したREDCapというデータ集積管理システムを用いて、国内各施設において臨床情報を登録します。登録された情報は暗号化され、JBCRGから委託を受けたサーバー会社のサーバーに保管され、管理されます。サーバーの選択はアクセスログ管理やセキュリティ対策、停電等の対策が行われていることを条件とします。
今後行われる臨床研究
このデータベースに保管される臨床情報を用いた臨床研究は、国の指針に基づいて次のように適正に行われます。
1.臨床情報は、適切な管理のもとに保管され、許可された者だけがその情報を見ることができる体制をとっています。
2.遺伝子に関する情報を含む医学研究への利用においては、国内の「人を対象とする生命科学・医学系研究に関する倫理指針」に基づいて行われます。
3.臨床研究で用いられた個人を識別できないよう加工された臨床データは、その研究代表者の責任のもとに保管されます。研究終了時から5年間は研究の信頼性、再現性を確保するために研究代表者のもとで厳重に保管されますが、その後は利用できない形で破棄されます。ただし、データの廃棄にあたっては、JBCRGより事前に各施設責任医師に対し通知を行い、各施設の患者さんのデータをcsv等のフォーマットでダウンロードする等の対応方法を連絡します。施設によりダウンロードされたデータは、施設の規程にしたがって適切に保管・利用・廃棄するものとします。
モニタリングや監査
このデータベースに保管されるあなたの臨床情報があなたのカルテ等に基づいて正しく記載・登録されているか、また、データベースの安全やこのプロジェクトに関する記録が適正に保たれているか等を確認することを目的に、JBCRGやJBCRGが委託する第三者が、モニタリングや監査を行うことがあります。これはプロジェクトの質を保持するために非常に重要なプロセスですが、その際、モニタリングや監査を行う人物が、医師の立ち会いのもと、あなたの診療情報や検査情報等にアクセスし、個人情報を閲覧する可能性があります。
しかしながら、その場合においても、JBCRGやJBCRGが委託する第三者が、個人を特定できる情報を記録したり、外部に持ち出したりすることはありません。
5.倫理審査委員会について
倫理審査委員会とは、臨床研究に参加される方の人権と安全性を確保しつつ、臨床研究の内容が科学的、倫理的に妥当であり、研究計画に問題がないかどうかを審査するための委員会のことです。
この委員会は、医療(医学や薬学)の専門家に加え、医療の専門家以外の学識経験を有する委員、当院と利害関係のない委員の参加が義務付けられており、研究計画内容の審査を行っています。
研究に臨床情報を利用できるか否かの判断は、JBCRGにおける審査と東海大学医学部臨床研究審査委員会で審査の上決定します。
東海大学医学部臨床研究審査委員会で実施が許可された研究は、JBCRG-ABCD projectという研究名でJBCRGや各施設のホームページに掲載されます。解析結果を個人の方に知らせることはありません。個々の研究計画について詳細を知りたいときは、担当医あるいはJBCRGの問い合わせ窓口へお申し出ください。
6.特許権・研究成果の帰属等について
この研究によって、特許に結びつくような発見があるかもしれませんが、それらによって生じた知的財産権や経済的な利益はJBCRGに帰属します。データベースに登録された情報は、JBCRGに帰属し、進行・再発乳がん患者さんの貴重なデータとして活用されます。ただし、データベースに登録された患者さんのうち、当院でこの研究に参加した患者さんの情報については、診療や教育に役立てる目的で、当院で活用することができます。この研究に参加していただいた患者さんが、これらの権利を主張することはできません。
この研究の研究成果は、学会や論文で発表が行われますが、これらの研究成果の発表で公開されるデータは、データベースに登録された多くの患者さんのデータの集計された数値や分析された結果となるため、個々の患者さんの診療情報や個人情報が特定されることはありません。
7.本プロジェクトにかかる利害の衝突・利益相反管理について
本データベースプロジェクトの運営に携わる研究運営組織代表者、研究代表者、実行委員、統計アドバイザーと医薬品等製造販売業者等との利益相反関係は、JBCRGの利益相反委員会にて審査を受けています。また、当院でこのデータベースプロジェクトに関与する研究者の利益相反については、当院の利益相反関連規程・利益相反マネジメントポリシーに従い、施設責任医師が管理します。
データベースにあなたを含めた患者さんの症例データを登録・集積し、そのデータを解析するにあたり、患者さんの診療等に使用した医薬品等の製造販売業者及びそれに関連する者を、そのデータ登録や解析に関与させることはありません。また、それらの医薬品等製造販売業者等に対し、本プロジェクトのデータベースやモニタリング記録等の資料、個々の患者さんに関する登録データ、個人情報を閲覧させることはありません。
本研究はJBCRGの資金により実施します。また、研究の実施・継続のために、公的資金や民間(企業を含む)の競争的資金や助成金、寄付金等による資金調達を行います。これらの資金提供元については、その資金提供元と研究者との関係を明確にするため、本研究の成果公表の際に公開されます。
このプロジェクトは以下の研究者と組織により実施されます。この研究について知りたい事や心配なことがありましたら、担当医にご遠慮なくおたずねください。
進行・再発乳癌データベースプロジェクト 研究代表者
東海大学医学部 外科学系 乳腺・腫瘍科学 新 倉 直 樹※
博愛会 相良病院 乳腺・甲状腺外科 相 良 安 昭
福島県立医科大学 腫瘍内科学講座 佐 治 重 衡
※印:共同研究機関の研究責任者を代表する研究責任者
施設責任医師
神鋼記念病院 科名:乳腺科 氏名: 松本 元
8.本プロジェクトに関する組織と相談窓口
本プロジェクトを統括する組織・データベース管理者
一般社団法人JBCRG(Japan Breast Cancer Research Group)
〒103-0016 東京都中央区日本橋小網町9-4
TEL:03-6264-8873 E-mail:ABCD-project@jbcrg.jp
代表理事 増 田 慎 三(京都大学大学院)
このプロジェクトについて何か聞きたいこと、相談したいことや苦情などがありましたら、担当医師又は下記の相談窓口までお問い合わせ下さい。
病院の相談窓口 TEL:078-261-6711 担当者: 松本 元
このデータベースプロジェクトについて十分ご理解いただけましたでしょうか。わからないこと、説明してほしいことがありましたら、遠慮なくご質問ください。
十分にご理解いただいたうえで、研究に参加することにご同意されましたら、次のページの同意文書に署名又は記名・捺印し、同意年月日を記入してください。署名又は記名・捺印後は、説明文書と同意文書の写しを必ずお受け取り下さい。
CT画像報告書の説明漏れを防ぐための組織的な取組みの検討
研究の対象
放射線科医師により作成されたCT画像報告書に記載された所見
研究期間
後向きの研究(調査対象期間2022年9月1日~2023年8月31日)
試料・情報の利用及び提供を開始する予定日
日本医療マネジメント学会学術雑誌への投稿予定
研究目的
CT報告書における要注意所見の伝達漏れを防止するための多職種連携型の仕組みを構築し、その有効性を検証することを目的とする。
研究方法
過去1年間(2022年9月より2023年8月まで)に撮影されたCT画像報告書を対象に、医療安全医師が要注意所見の有無を判定し、該当症例についてカルテ記載の有無を調査した。あわせて、診療情報管理士によるキーワード検索および放射線科医師による重要所見へのフラグ付けを実施し、3つの手法の有効性を検証した。
研究に用いる試料・情報の種類
放射線科医師により作成されたCT画像報告書
情報の保存・保護
研究関連文書は施錠された場所に保管し、研究終了後は終了報告書と共に研究事務局に提出します。保管期間は研究終了報告日から5年、または研究結果の最終公表日から3年のいずれか遅い日までとし、その後は適切に廃棄します。
外国にある者に対して試料・情報の提供する場合
本研究では、試料や情報の提供先は国内に限られており、外国に対して試料や情報を提供する予定はありません。
利益相反
本研究に関与する全ての研究者は、研究に関連する経済的または個人的な利益相反がないことを確認しています。研究は独立して実施され、外部からの影響を受けないことを保証する。
本研究への参加を希望されない場合
本研究は、病院内の全てのCT報告書を対象としたもので、参加は必須です。研究に参加しない選択肢はありませんが、個人情報の取り扱いや患者様の権利は適切に保護されます。
お問い合わせ先
神鋼記念病院 医療安全管理室
担当:上原 徹也(研究責任者)
電話:078-261-6711(代表)
受付時間:平日 9:00〜17:00(土日祝を除く)
当院におけるがん遺伝子パネル検査を受ける患者の現状と看護の課題
当院では、2023年1月にがんゲノム医療連携病院に認定され、同年3月からがんゲノム診療科を開設しました。2025年3月までに53名の患者さんが、がん遺伝子パネル検査(CGP)を受けられました。
CGP検査とは、がん細胞の遺伝子の変化に対応する治療薬があるかどうかが分かる検査です。日本では、2019年にCGP検査が医療保険で受けられるようになりました。しかしながら、CGP検査を受けることが出来る対象者は、限られており、検査費用も高額であるのが現状です。また、CGP検査を受けても必ずしも新たな治療薬が見かる訳ではないのが現状です。
このたび、CGP検査を受けた患者さんの身体・心理・社会面を診療録から調査し、患者さんの現状や課題を明らかにして、看護に役立てたいと考えています。つきましては、この研究の対象者にあたると思われる方でご質問のある方、またはこの研究にご自身の診療情報を使用して欲しくないとお考えの場合は、遠慮なく下記の担当者までご連絡頂きますようよろしくお願い申し上げます。
研究の目的・意義
CGP検査を受けた患者さんの身体・心理・社会面を診療録から調査し、患者さんの現状や課題を明らかにし、患者さんに必要な看護に役立てることです。
情報の取得期間
2023年3月1日~2025年3月31日
利用する診療情報の項目・内容
年齢、性別、病状の経過、疾患名、がんのステージ、身体活動状況、治療期間、情報源、推奨された治療、提案された薬剤の費用負担の種類、検出された遺伝子変異、二次的所見結果、推奨治療の実施、CGP検査に対する理解、二次的所見の開示希望、職業、キーパーソン、社会資源の活用、健康保険
個人情報の保護
個人情報に関する取扱いの際は、厳重に管理いたします。研究者以外の第三者に個人情報が流出することはありません。また、この研究結果に関する内容を学会で発表する際には、個人が特定されるような形で使用いたします。
利益相反
本研究における、会社や個人との利益相反はありません。本研究への参加を拒否される場合は、当院の下記担当者までご連絡ください。なお、拒否のお申し出による患者様・ご家族様への不利益は生じないことを保障いたします
お問い合わせ先
住 所:〒651-0072 神戸市中央区脇浜町1-4-47
電 話:078-261-6711 FAX:078-261-6726
担当者:がんゲノム診療科看護師 高岡 貴子
術前主膵管径3mm以下で柔らかい膵実質を持つ症例における膵液瘻リスク因子の同定:DAIMONJI-Study事後解析
消化器外科を受診中の患者さんへ
現在消化器外科では、下記の臨床研究を実施しております。
この研究では、患者さんの日常診療で得られた試料・情報を利用させていただきます。
ご自身の試料・情報がこの研究に利用されることについて、異議がある場合は、試料・情報の利用を停止することができます。ただし、すでに研究結果の解析が終了し、公表されている場合などに、あなたの情報のみを取り除くことができない可能性もあります。研究の計画や内容などについて詳しくお知りになりたい方、ご自身の試料・情報がこの研究で利用されることについて異議のある方、その他ご質問がある方は、以下の「問い合わせ先」へご連絡ください。
研究課題名
術前主膵管径3mm以下で柔らかい膵実質を持つ症例における膵液瘻リスク因子の同定:DAIMONJI-Study事後解析
研究の目的
2017年10月から2020年7月までに当院で膵頭十二指腸切除術を行った患者さんを対象に、通常の診療で得られた試料・情報を収集・解析します。その結果、術後合併症である膵液瘻がおこりやすい因子を同定し、より安全な手術方法を確立することを目的としています。
対象となる患者さん
2017年10月から2020年7月までに当院で膵頭十二指腸切除術を行った患者さんで、膵管の太さが3mm以下で、かつ手術中に評価した膵臓の硬さが「柔らかい」と主治医が判断した患者さん。
研究予定期間
2025年 1月20日※から 2026年 1月20日
※ただし、病院長の許可日以降に開始します
研究機関の長
国立病院機構京都医療センター 病院長 小池薫
使用させていただく試料・情報
・年齢、性別、身長、体重
・病名、重症度
・手術の情報
・術後経過
・CT画像 等
個人情報の取り扱いと倫理的事項
研究に利用する試料・情報は、患者さんを直接特定できる情報(お名前やカルテ番号など)を削除し加工しますので、当院のスタッフ以外が当院の患者さんを特定することはできません。
この研究成果は学会や学術雑誌などで発表することがありますが、その場合でも上記のとおり加工していますので、患者さんのプライバシーは守られます。
なお、この研究は、国の定めた指針に従い、当院の研究倫理審査委員会の審査・承認を得て、病院長の許可のもと実施しています。
研究機関(情報管理責任者)および問い合わせ先
国立病院機構京都医療センター
研究責任者 外科医長 中村公治郎
研究分担者 研究員 成田匡大
住所:京都市伏見区深草向畑町1-1
電話:075-641-9161
・神鋼記念病院への問い合わせ先
消化器外科 医長 光岡英世
住所:神戸市中央区脇浜町1-4-47
電話:078-261-6711
免疫チェックポイント阻害薬投与終了後に新規発症する遅発性甲状腺機能障害についての後方視的研究
当院では、以下の臨床研究を実施しております。この研究は、日常診療で得られた以下の診療情報を研究データとしてまとめるものです。研究のために、新たな検査などは行いません。この案内をお読みになり、ご自身またはご家族がこの研究の対象者にあたると思われる方で、ご質問がある場合、またはこの研究に診療情報を使ってほしくないとのご意思がある場合は、遠慮なく下記の担当者までご連絡ください。
ただし、すでに解析を終了している場合には、研究データから情報を削除できない場合がありますので、ご了承ください。
対象となる方
当院において、2017年4月1日より2025年3月31日までに肺がん、乳がん、膀胱がん、悪性リンパ腫、腎がん、胃がん、肝細胞がん、食道がん、胆管がん、膵がん、悪性中皮腫と診断され、免疫チェックポイント阻害薬と呼ばれるニボルマブ、イピリムマブ、ペンブロリズマブ、アテゾリズマブ、デュルバルマブ、トレメリムマブのいずれかの薬剤の投与を受けられた方を対象としています。
研究代表者
神鋼記念病院 診療技術部薬剤室 刈谷 美里
研究の目的
免疫チェックポイント阻害薬の一般的な副作用の一つに甲状腺機能障害があります。そのため、免疫チェックポイント阻害薬による治療中は、定期的なTSHやFT4のモニタリングが推奨されています。しかし、免疫チェックポイント阻害薬による治療終了後も遅発性に甲状腺機能障害が発症する可能性があることが知られていますが、検査値のモニタリングについて明確な基準はありません。本研究は、免疫チェックポイント阻害薬の投与を終了した方を対象に調査を行い、甲状腺機能障害の発生率および危険因子を検索し、免疫チェックポイント阻害薬による副作用管理の向上に寄与することを目的としています。
利用する診療情報
免疫チェックポイント阻害薬を含む化学療法を受けた患者の年齢、性別、がん種、前治 歴、後治療、既往歴、合併症、使用したICIの種類、脳転移の有無、併用薬 、TSH、 FT3、FT4、TPOAb、TgAbを診療録から集積し解析します。
研究期間
2017年4月1日より2025年3月31日まで(予定)
個人情報の取り扱い
お名前、住所などの個人を特定する情報につきましては厳重に管理を行い、学会や学術雑誌等で公表する際には、個人が特定できないような形で使用いたします。
この研究で得られた情報を将来、他の研究機関に提供し二次利用する場合や、研究計画書を変更する場合があります。その場合は、研究倫理審査委員会での審議を経て、研究統括管理責任者の許可を受けて実施されます。その際、文書を公開する場合は、神鋼記念病院 公式サイト(https://shinkohp.jp/)の「患者・ご家族の皆様へ 研究情報の公開について」のページに掲載いたします。
問合せ先
神鋼記念病院薬剤室 刈谷 美里
〒651-0072 兵庫県神戸市中央区脇浜町1丁目4−47
TEL 078-261-6711 FAX 078-261-674
造血器疾患における遺伝子異常の網羅的解析研究
研究の目的
血液感染症を含むすべての造血器疾患を対象として遺伝子解析を行いその疾患の発症、進行、治療への影響を検討します。また将来的に新しい解析技術が開発された場合に備えて検体を保存します。
研究期間
2015/2/10 ~ 2028/3/31
※遵守すべき指針やガイドラインの改正に合わせ、適宜研究計画の改定・延長を行います。
倫理審査委員会の審査を受け、研究機関の長の許可を受けている
今回の研究は京都大学医学部附属病院の「医の倫理委員会」で審査され病院長により承認を受けています。京都大学血液・腫瘍内科が主体となり多くの共同研究機関と協力して行います。ご提供いただいた検体は、研究用のコード番号で管理し、ご提供いただいた方の個人情報が研究利用の段階で漏えいすることがないよう管理します。また、研究協力を辞退されても診療上の不利益を被ることはありません。
研究機関の名称・研究責任者の氏名
京都大学医学部附属病院 血液内科 高折晃史
試料・情報の利用目的・利用方法
いただいた検体を使って京都大学もしくは国内、海外の共同研究機関で遺伝子解析などの研究が行われます。遺伝子解析とは次世代シークエンサーなどの新しい機械を用いた全ゲノム解析を含む網羅的遺伝子解析のことです。これにより全ての遺伝子の異常を詳細に調べることができ、今まで知られていなかった遺伝子と病気の関係を調べることができます。全ての遺伝子が対象となりますが、血液の病気の発症や進展にまったく関係のない遺伝子を調べることはありません。遺伝子解析をすぐに行わない場合には当科の冷凍庫で長期保存します。長期保存された検体は様々な医学・医療の発展に資する取り組みに活用され、さらに薬事申請など実用化普及を通じて、医学研究・教育・医学の発展のために使用されます。また網羅的遺伝子解析の結果や臨床情報は公的データベースに登録される場合があります。 G608「造血器腫瘍における遺伝子異常の網羅的解析」研究に使用されたゲノム由来データおよび診療情報はセキュリティの担保された方法によって、東京大学医科学研究所ヒトゲノム解析センターや国立がん研究センターが整備するストレージやセキュリティの担保された公共クラウドシステムに送付・保管され、許可されたもののみがアクセスし解析を行います。具体的には「令和3年度「革新的がん医療実用化研究事業」【領域1-14】「がん全ゲノム解析等におけるゲノム解析・臨床応用に関する研究」の研究班、および関連する研究従事者で構成される「解析・データセンター」が行います。
利用または提供する試料・情報の項目
通常の方法で採血します。また、この病気のために検査・手術を受ける場合には、取り出された組織(骨髄やリンパ節など)を使う場合もあります。通常の検査に必要な血液や骨髄液の残りをいただきますので研究にともなう身体の危険性は全くありません。病気によって診断に必要な検査の際に、追加して検体を採取させていただく場合があり、その場合、貧血などの問題が起こらないように十分に配慮して血液10〜50ml、骨髄液5〜10ml、尿10〜20mlの提供をお願いしています。頬粘膜検体(口の中をスポンジで軽くぬぐい採取します)の提出をお願いすることがあります。また、初診時だけでなく治療中、治療後の検体の提供をお願いする場合があります。 遺伝子と症状の関係を知るためにあなたの病気の症状を通常通りカルテに記録していきます。今後、研究のために症状を調査する場合にカルテを参考にします。
当該研究を実施する全ての共同研究機関の名称及び研究責任者の氏名
研究を共同で行う機関・責任者名について
―学内研究室―
・京都大学大学院医学研究科 腫瘍生物学 教授 小川 誠司
・京都大学大学院医学研究科 臨床病態検査学 教授 長尾 美紀
・京都大学大学院医学研究科 医科学 教授 竹内 理
・京都大学iPS細胞研究所 臨床応用研究部門 教授 斎藤 潤
・京都大学iPS細胞研究所 臨床応用研究部門 助教 丹羽 明
・京都大学iPS細胞研究所 未来生命科学開拓部門 齊藤 博英
・京都大学医学領域産学連携推進機構 准教授 渡辺 亮
・京都大学高等研究院ヒト生物学高等研究拠点 (ASHBi) 特定拠点准教授 山本 玲
・京都大学高等研究院ヒト生物学高等研究拠点 (ASHBi) 教授 村川 泰裕
―国内大学―
・東京大学医学部附属病院 小児科 教授 加藤 元博
・東京大学医学部附属病院 血液腫瘍内科 教授 南谷 泰仁
・東京大学医科学研究所 感染症国際研究センター システムウイルス学 教授 佐藤 佳
・慶應義塾大学病院 血液内科 教授 片岡 圭亮
・聖マリアンナ大学 医療情報実用化マネジメント学寄附研究部門 教授 渡邉 俊樹
・日本医科大学付属病院 血液内科 教授 山口 博樹
・金沢大学 血液内科 呼吸器内科 教授 宮本 敏浩
・金沢大学 血液病態検査学 教授 森下 英理子
・名古屋大学大学院 微生物免疫学講座ウイルス学分野 教授 木村 宏
・愛知学院大学 薬物治療学講座 教授 加藤 宏一 講師 加藤 文子
・東邦大学 薬学部 病態生化学研究室 教授 檜貝 孝慈 准教授 巽 康彰
・同志社大学 生命医科学部 医生命システム学科 助教 高橋 美帆
・大阪大学免疫学フロンティア研究センター 実験免疫学 教授 坂口 志文
・奈良県立医科大学 小児科 准教授 野上 恵嗣
・神戸大学大学院医学研究科 内科学講座 小児科学分野 造血幹細胞医療創成学部門 特命教授 宮西正憲
・岡山大学病院 ゲノム医療総合推進センター 准教授 遠西 大輔
・岡山大学大学院医歯薬学研究科病態制御科学専攻腫瘍制御学講座 血液・腫瘍・呼吸器内科学分野 教授 前田 嘉信
・川崎医科大学 検査診断学 教授 通山 薫
・広島大学大学院医系科学研究科 ウイルス学研究室 准教授 入江 崇
・九州大学病院 血液・腫瘍・心血管内科 診療准教授 加藤 光次
・九州大学別府病院 内科 教授 堀内 孝彦
・宮崎大学農学部獣医学科 獣医微生物学研究室 准教授 齊藤 暁
・琉球大学医学研究科 皮膚病態制御学講座 教授 高橋 健造
―国内研究所―
・理化学研究所 生命医科学研究センター理研-IFOMがんゲノミクス連携研究チーム
チームリーダー 村川 泰裕
・国立がん研究センター 中央病院 造血幹細胞移植科 科長 福田 隆浩
・国立がん研究センター研究所 鶴岡連携研究拠点 がんメタボロミクス研究室
チームリーダー 横山 明彦
医薬品食品衛生研究所 安全生物試験研究センター 薬理部 部長 諫田 泰成
・国立長寿医療研究センター 理事長 荒井 秀典
・ヒトレトロウイルス学研究センター
ゲノミクス・トランスクリプトミクス学分野 教授 佐藤 賢文
感染免疫学分野 教授 上野 貴将
分子ウイルス・遺伝学分野 准教授 池田 輝政
―海外研究機関―
・Campbell Family Institute for Breast Cancer Research, University of Toronto, Tronto, Ontario, Canada
Director and Professor, Tak W. Mak, PhD
・FIRC Institute of Molecular Oncology, Milan, Italy
Principal Investigator, Stefano Casola, MD, PhD
・IRCCS San Raffaele Scientific Institute, Milan, Italy. Luca Vago MD, PhD
※カナダでは個人情報保護及び電子文書法およびプライバシー法による個人情報の保護に関する制度を有しています。EU加盟国では日本の個人情報保護委員会より我が国と同等の水準にあると認められる個人情報の保護に関する制度を有しています。
―国内企業―
・レパトア・ジェネシス株式会社 代表取締役社長 鈴木 隆二
・公益財団法人HLA研究所 所長 田中 秀則
・ジェノダイブファーマ株式会社 代表取締役社長 細谷繁
・合同会社H.U.グループ中央研究所 社長付け 担当部長 今村健一
・株式会社サイバーオミックス 代表取締役社長 渡辺亮
・タカラバイオ株式会社 代表取締役社長 仲尾 功一
・株式会社マクロジェン・ジャパン 代表者 安 光得、金 尚完
・株式会社理研ジェネシス 代表取締役社長 岩壁 賢治
・株式会社ハプロファーマ 代表取締役社長 大滝 義博
・スタンダードバイオツールズ株式会社 代表取締役社長 板谷 英貴
※患者情報は提供されず、UPNを付与し仮名化した検体のみを提供する。UPNとの一覧表は京大内で作成し、外部委託先に提供はしません。
検体の採取を共同で行う機関・責任者名について
・自治医科大学附属病院 血液科 教授 神田善伸
・自治医科大学附属さいたま医療センター 血液科 教授 神田善伸
・静岡県立総合病院 血液内科部長 野吾 和宏
・地方独立行政法人静岡市立静岡病院 血液内科 医長 山崎寛章
・市立島田市民病院 血液内科主任部長 柳田 宗之
・焼津市立総合病院 小児科 科長 熊谷淳之
・名古屋市立大学 血液・腫瘍内科 教授 飯田 真介、准教授 李 政樹
・大津赤十字病院 血液内科部長 辻 將公
・滋賀県立総合病院 血液腫瘍内科科長 浅越 康助
・京都医療センター 血液内科医長 川端 浩
・京都桂病院 血液内科統括部長 菱澤 方勝
・京都市立病院血液内科部長 伊藤 満
・医仁会武田総合病院 血液内科センター長 中坊 幸晴
・日本バプテスト病院 血液内科部長 小林 正行
・洛和会音羽病院 血液内科部長 石橋 孝文
・宇治徳洲会病院 血液内科部長 安齋 尚之
・天理よろづ相談所病院 血液内科部長 赤坂 尚司
・高の原中央病院 血液内科 部長 石川隆之
・日本赤十字社和歌山医療センター 血液内科部長 岡 智子
・高槻赤十字病院 血液内科部長 前迫 善智
・社会福祉法人大阪府済生会野江病院 血液リウマチ内科部長 金子 仁臣
・大阪赤十字病院 血液内科部長 今田 和典
・公益財団法人田附興風会医学研究所北野病院 血液内科主任部長 北野俊行
・関西電力病院血液内科部長 井尾 克宏
・兵庫県立尼崎総合医療センター 血液内科科長 渡邊 光正
・社会医療法人神鋼記念病院 血液病センター長 有馬 靖佳
・神戸市立医療センター中央市民病院 血液内科部長 石川 隆之
・倉敷中央病院 血液内科部長 上田 恭典
・一般財団法人平成紫川会小倉記念病院 血液内科部長 米澤 昭仁
・長崎大学病院 血液内科 教授 宮崎 泰司
・佐賀大学医学部附属病院 血液・呼吸器・腫瘍内科 教授 木村 晋也
試料・情報の管理について責任を有するものの氏名又は名称
京都大学血液・腫瘍内科学 教授 高折晃史
試料・情報の利用または提供を開始する予定日
当院の研究実施許可日
研究対象者又はその代理人の求めに応じて、研究対象者が識別される試料・情報の利用又は他の研究機関への提供を停止すること
外部研究機関への検体の提供について
本研究は京都大学以外の共同研究機関でも遺伝子解析を予定しています。また、今後、研究計画に参加している研究者以外の研究者から、あなたの検体や診療情報を使用したいという申込みがある可能性もあります。その場合、外部研究機関の倫理委員会で審査・承認された研究計画にしたがって検体が取り扱われる場合に限ってあなたの検体を提供させて頂きたいと考えています。また営利企業を含む外部検査機関に遺伝子解析を委託する場合があります。後日、同意の取り消しを希望された場合、外部研究機関に連絡して使用を中止することが出来ます。
細胞バンクへの検体の提供について
あなたの検体を用いて細胞株が作成された場合、多くの研究者が利用して研究が速やかに進むように細胞バンクに提供する場合があります。細胞バンクとは様々な細胞を登録・保管し、申込みに応じて、必要な細胞を各研究機関に送付する作業を行う専門の施設です。あなたの個人情報は保護され、さらにバンクから外部研究機関へ細胞が提供される際も当然、あなたの個人情報は保護されます。ただし、細胞バンクから外部研究機関への提供後には同意の撤回をしたくても、その取り消しはできなくなります。
亡くなった研究対象者の試料・情報の利用について
血液疾患は稀少疾患(患者さんの人数が非常に少ない疾患群)のため、患者さんの試料と臨床情報が非常に貴重です。今後の血液疾患の治療の発展に役立てるため、既に亡くなられた患者さんのうち、検体の診療目的外利用に明らかな不同意を示されていない方の保存試料及び電子カルテ情報を本研究の対象とさせていただく場合があります。患者さんが亡くなられて時間が経っている場合など、ご家族へ連絡することが難しい場合には、ご家族の了承を確認せずに試料及び診療情報を使用させていただく可能性があります。試料及び診療情報の利用の停止を希望されるご家族は下記連絡先までご連絡下さい。
他の研究対象者等の個人情報及び知的財産の保護等に支障がない範囲内での研究に関する資料の入手・閲覧およびその方法
検体の利用状況に関する情報公開を京都大学血液・腫瘍内科学講座ホームページで行っています。
http://www.kuhp.kyoto-u.ac.jp/~hemonc/research/content/G697.html
当科で新しい研究が開始される場合はその概要がホームページ上に掲示されます。
利益相反について
この研究は、公的研究費である日本医療研究開発機構(AMED)研究費、日本学術振興会(JSPS)科学研究費助成事業研究費、奨学寄附金により実施します。また、本研究は、現在、特定の企業からの資金提供を受けておりませんが、今後、提供を受ける場合も資金提供者の意向が研究に影響することはありません。
利益相反については、「京都大学利益相反ポリシー」「京都大学利益相反マネジメント規程」に従い、「京都大学臨床研究利益相反審査委員会」において適切に審査しています。
利益相反に関する情報公開も上記ホームページで行っています。
研究対象者及びその関係者からの求めや相談等への対応方法
遺伝カウンセリングの体制について
病気のことや遺伝子解析に関して、不安に思うことや相談したいことがある場合は、遺伝カウンセリング担当者が相談を受けます。診療を担当する医師、インフォームド・コンセント担当者など病院職員にその旨お伝えください。
京都大学医学部附属病院遺伝子診療部:予約制、電話075-751-4350
問合せ・苦情・参加辞退の受付先
説明の中でわからない言葉や質問、また参加や結果開示のことで相談がありましたら何でも遠慮せずにご連絡ください。
血液・腫瘍内科学講座 (電話 075-751-4964)
京都大学医学部附属病院 臨床研究相談窓口
(Tel)075-751-4748 (E-mail) ctsodan@kuhp.kyoto-u.ac.jp
神鋼記念病院 (電話 078-261-6711)
血液内科 田中 康博
他以下を記載、公開しています。
・結果の公表について
この研究によって成果が得られた場合は、国内外の学術集会・学術雑誌などで公表します。その際にも、ご提供者の個人情報が明らかになることはありません。
・関連する研究番号と課題名
この研究は以下の研究と関連実施しています。あわせてご参照ください。
G608 造血器腫瘍における遺伝子異常の網羅的解析
G1010 アグレッシブATL前向きコホート研究、附随研究/検体バンキング
G1021 ドナー細胞由来造血器腫瘍の発症に関わる分子機構の解明
G1026 非血縁者間骨髄・末梢血幹細胞移植における検体保存事業
また、この研究と連携して、今後倫理審査を経て研究が応用される可能性があります。倫理審査が終了した研究課題については、随時ホームページに公開いたします。
血液中miRNA測定による消化器癌の診断法確立に向けた研究
2020年11月18日から2023年12月19日の間、「血液中 miRNA 測定による消化器癌の診断法確立に向けた研究」に参加いただいた方へ
新たにご協力いただきたいこと
同定された有用な短鎖 RNA を用いた膵癌、胆道癌、肝癌の診断法および診断補助法の実用化に向けて、あなたの研究参加により採取した生体試料中の短鎖 RNAの測定に加えて、各種腫瘍マーカー(CA19-9, CEA, DUPAN2, AFP, PIVKA-2, AFP-L3, SCC, CYFRA等)を測定し、解析させてください。また、生体試料の測定結果および関連する診療情報を薬事等の承認申請のために利用させてください。あなたの生体試料および関連する診療情報の薬事等の承認申請への使用を拒否されたい場合は、文末の問い合わせ先までご連絡ください。拒否された場合でも、何ら不利益を受けることはありませんし、それ以降患者さんのデータを本研究に用いることはありません。しかしながら、すでに研究成果が論文などで公表されていた場合のように、結果を廃棄できない場合もあります。
研究の目的・意義
本研究は、血液中のmiRNAを測定することによって膵癌、胆道癌、肝癌の発症を早期に診断するためのマーカーを同定し既存の診断手法よりも精度良く早期に膵癌、胆道癌、肝癌を診断する手法の確立に繋げることを目的とします。
研究実施期間
2020年11月18日より2029年12月31日まで
対象となる試料・情報の取得期間
2020年11月18日から2023年12月19日の間に、「血液中 miRNA 測定による消化器癌の診断法確立に向けた研究」(京都大学倫理委員会承認番号:R2692)に参加いただいた方は、以下の方になります。 ◆京都大学医学部附属病院消化器内科および肝胆膵・移植外科/小児外科もしくは共同研究機関において、膵癌、胆道癌、肝癌の罹患が強く疑われ、検査や治療目的で来院した患者さんのうち「血液中 miRNA 測定による消化器癌の診断法確立に向けた研究」への参加に同意をいただいた方 ◆アークレイ株式会社にて試料・情報を採取した癌患者群背景がおよそ合致する健常者の方 ◆京都大学医学部附属病院消化器内科および肝胆膵・移植外科/小児外科もしくは共同研究機関に検査や治療目的で来院し、膵癌との鑑別が必要となるその他の膵腫瘍および膵炎(慢性膵炎、自己免疫性膵炎など)の罹患が強く疑われる患者さん、並びに、胆道癌との鑑別が必要になる胆道疾患(IgG4 関連疾患、原発性硬化性胆管炎)、及びその他の良性疾患(総胆管結石など)の罹患が強く疑われる患者さん、並びに、肝癌との鑑別が必要になる肝良性腫瘍(肝細胞腺腫など)、及びその他の良性疾患(肝硬変、B 型慢性肝炎、C 型慢性肝炎、非アルコール性脂肪肝炎、アルコール性肝炎など)の罹患が強く疑われる患者さんのうち「血液中 miRNA 測定による消化器癌の診断法確立に向けた研究」への参加に同意をいただいた方、及び同意を得られた患者さんのうち、手術または化学療法を受けた方
利用または提供を開始する予定日
研究機関の長の実施許可日以降
利用または提供する試料・情報の項目
利用または提供する試料は血清 利用または提供する情報は年齢、性別、身長、体重、採血日時、採血前食事時間、診断名、病理組織診断名、腫瘍径、臨床病期、TNM分類、原発部位、各種腫瘍マーカー(CA19-9, CEA, DUPAN2, AFP, PIVKA-2, AFP-L3, SCC, CYFRA)、既往歴、服薬状況、喫煙歴、飲酒歴、家族の癌罹患歴、化学物質暴露歴等
試料・情報の管理について責任を有する者の氏名または名称
福田 晃久(ふくだ あきひさ)
研究資金・利益相反
この臨床研究に関する研究資金は共同研究先であるアークレイ株式会社から受け入れる研究費より支出される。血液検体採取・miRNA解析に関わる費用は、共同研究先であるアークレイ株式会社が負担する。研究において、開示すべき利益相反は上記のみである。利益相反については、「京都大学利益相反ポリシー」「京都大学利益相反マネジメント規程」に従い、「京都大学臨床研究利益相反審査委員会」において適切に審査する。
当該研究を実施する研究機関の名称及び研究責任者の氏名(機関名/責任者/職名)
神鋼記念病院 消化器内科・医長・生田 耕三
この研究は以下の施設と共同研究を行っています。
(共同研究機関の名称 研究責任者の所属・職位・氏名)
アークレイ株式会社 研究開発本部開発七部第一チーム・責任者・平井 光春
京都大学医学部附属病院/福田 晃久/消化器内科 准教授
京都府立医科大学大学院医学研究科病態分子薬理学・教授・楳村 敦詩
天理よろづ相談所病院 消化器内科・医員・南 竜城
北野病院 消化器内科・医員・森田 敏広
大津赤十字病院 消化器内科・医員・益田 朋典
兵庫県立尼崎総合医療センター 消化器内科・医長・山内 雄揮
神戸市立医療センター中央市民病院 消化器内科・医長・和田 将弥
大阪赤十字病院 消化器内科・副部長・浅田 全範
日本赤十字社和歌山医療センター 主任部長・上野山 義人
近畿大学病院 消化器内科・准教授・渡邉 智裕
神戸市立西神戸医療センター 消化器内科・副医長・髙田 裕
高槻赤十字病院 消化器科・副部長・吉岡 拓人
神鋼記念病院 消化器内科・医長・生田 耕三
京都桂病院 消化器内科・副部長・中井 喜貴
滋賀県立総合病院 消化器内科・科長・松村 和宜
京都第一赤十字病院 消化器内科 部長・佐藤 秀樹
市立大津市民病院 消化器内科 診療部長・髙見 史朗
近江八幡市立総合医療センター 消化器内科 部長・石川 博己
京都市立病院 消
研究対象者およびその関係者からの求めや相談等への対応方法
1) 研究機関相談窓口
福田 晃久(ふくだ あきひさ)
〒606-8507 京都市左京区聖護院川原町54
京都大学医学部附属病院 消化器内科
電話番号: 075-751-4319
Fax番号: 075-751-4303
2) 京都大学医学部附属病院 臨床研究相談窓口
電話番号:075-751-4748
E-mail:ctsodan@kuhp.kyoto-u.ac.jp
3) 神鋼記念病院の相談等窓口
神鋼記念病院 消化器内科
電話番号:078-261-6711
肺高血圧症発症や増悪のリスク因子を同定するための後方視的検討
本件は「オプトアウト」すなわち、同意不要であった既存データを用いた研究において、「自分のデータは使わないでほしい」という、患者さんの拒否の機会を確保するため、研究の公開をホームページ上で行っているものです。 今回の研究に該当されることが予想され、「自分のデータは使わないでほしい」と希望される方はご本人・ご家族より当院に手紙、メール、お電話もしくはファックスなどにてその旨ご連絡ください。
神鋼記念病院に通院・入院し、精査のために右心カテーテルを受けたことのある患者さんへ
実施する臨床研究
肺高血圧症を有していないか右心カテーテル検査を受けたことがある患者さんの診療経過について調査研究を実施しております。この研究は「観察研究」と呼ばれるもので、 通常の診療で得られた記録をまとめることによって行います。以下の点をご理解いただき、ご協力いただきますようお願い申し上げます。
この研究の意義、目的、および方法
肺高血圧症は早期診断が困難な疾患ですが、進行すると寿命に影響する疾患です。しかしながら、将来肺高血圧を発症するかどうか、治療中に悪化しないかどうかを事前に予測する方法はあきらかとなっていません。肺高血圧が疑われた患者さんの診療経過を調査し、その方法を確立することは、より正確な予後の予測や、適切な治療介入につなげるために重要であると考えられます。本研究では肺高血圧症が疑われ右心カテーテル検査を施行された症例を対象として、これまでの患者背景情報、各種検査結果、治療経過などを調査し解析します。
この研究による医学上の貢献と予測
日常臨床で得られる情報を通して、肺高血圧を将来発症したり治療にも関わらず悪化してしまったりする方にどのような因子があるのかを見出します。
この研究による患者さんの不利益および危険性
患者さんの診療情報を分析する研究であり、プライバシーも厳重に保護されますので、患者さんに不利益や危険性はありません。
費用や追加の検査
通常の保険診療による画像診断情報と臨床情報の収集と分析ですので、患者さんに余分な費用を負担してもらうことはありません。また、検査方法の変更や追加検査もありません。
個人情報の保護
この研究で得た情報は厳重に管理され、学術目的のみで利用されます。 研究結果は主として統計として処理・解析され発表されるため、個人を特定できることはありません。研究結果の発表に際して、一部の患者さんの臨床情報が参考所見として呈示される可能性がありますが、匿名化されていますので、個人を特定できることはありません。 本研究参加者以外の第三者に流出することもありません。以上のように、患者さんのプライバシーは厳重に保護されますのでご安心ください。
ご協力の拒否について
この研究にご自分のデータが使用されることを拒否される場合は、担当医もしくは下記の問い合わせ先に連絡下さい。 たとえ、協力を拒否されても、今後の診療の不利益になることはありません。しかし、拒否のお申し出のあった時点で、 既に研究結果が論文などで公表されていた場合には、 研究結果を破棄できないことがあります。 この場合でも個人が特定されることはありませんので個人情報は保護されます。
研究責任者
神鋼記念病院 呼吸器内科 稲尾 崇
当院における連絡先
神鋼記念病院 呼吸器内科 稲尾 崇
〒651-0072 神戸市中央区脇浜町1丁目4-47
TEL:078-261-6711 ・ FAX:078-261-6931
当院で入院中に嚥下調整食の提供を受けられた患者様・ご家族様へ研究へのご協力のお願い
当院では、栄養状態の低下やそのリスクがある入院中の患者様に対し、栄養サポートチームの介入を行っております。2024年度の取り組みとして、患者様の嚥下機能に合わせたお食事(以下、嚥下調整食と称します)の提供状況の確認と安全な食事継続に向けたサポートを開始いたしました。このたび、嚥下調整食の内容や今後の課題の明確化、さらに栄養サポートチーム介入による成果を評価するため、過去の診療録やチームの回診記録を研究データとしてとりまとめたいと考えています。この研究において新たに患者様の健康に関する新たな結果が得られるものではありません。
つきましては、この研究の対象者にあたると思われる方でご質問のある方、またはこの研究にご自身の診療情報を使用して欲しくないとお考えの場合は、遠慮なく下記の担当者までご連絡頂きますようよろしくお願い申し上げます。
研究の目的・意義
嚥下調整食の内容や今後の課題の明確化、さらに栄養サポートチーム介入による成果を明らかにすることです。それらを明確化することによって、入院患者様のさらなる栄養状態の改善や栄養状態低下の予防に貢献でき、疾病回復への一助となる可能性があると考えています。
情報の取得期間
2024年4月1日~2024年9月30日
利用する診療情報の項目・内容
年齢、性別、身長、体重、入院診療科、嚥下調整食の種類、喫食量、食事以外の栄養投与量(静脈・経腸栄養)、嚥下機能、口腔内の状態、食欲の有無、食事介助の有無・程度、食事時間、ラウンド中の指導内容、検査データ(血清Alb値)
個人情報の保護
診療録をはじめ個人情報に関する取扱いの際は、部外へ漏洩しないよう厳重に管理いたします。また、栄養サポートチームの介入に関する内容を学会で発表することもありますが、その際は、個人情報が特定できないよう匿名とし、治療内容やその経過から個人が推測されるような内容を含まないよう配慮いたします。
利益相反
本研究における、会社や個人との利益相反はありません。
本研究への参加を拒否される場合は、当院の下記担当者までご連絡ください。
なお、拒否のお申し出による患者様・ご家族様への不利益は生じないことを保障いたします。
お問い合わせ先
住 所:〒651-0072 神戸市中央区脇浜町1-4-47
電 話:078-261-6711 FAX:078-261-6726
担当者:NST看護師/摂食嚥下障害看護認定看護師 切通 京子(3北病棟)
管理栄養士 田中 利幸(栄養室)
慢性移植片対宿主病に対する体外フォトフェレーシス治療の有効性に関する検討
研究の目的・意義
同種造血幹細胞移植後の合併症である慢性移植片対宿主病(graft-versus-host disease; GVHD)は、口内炎や皮疹、肝障害など様々な症状を起こし、患者の生活の質を低下させるため、その制御は重要な課題となっています。慢性GVHDに対する標準的な一次治療は副腎皮質ステロイドですが、ステロイド抵抗性・不耐容の場合、標準的な二次治療法は確立されていません。2023年3月に、ステロイド抵抗性・不耐容慢性GVHD治療のための体外フォトフェレーシス(extracorporeal photopheresis;ECP)装置が保険適用となり、新たな治療選択肢に加わりました。ECPは、患者さんの血液を体外循環させながら、遠心分離により白血球を分離し、紫外線照射後に体内に戻すことで、免疫を調節してGVHD症状を改善します。海外では本治療により約6割の患者さんで症状の改善がみられると報告されています。日本においても、今後のより良い慢性GVHD治療のために、ECP治療の有効性と安全性を確認していくことが必要と考え、この臨床研究を計画しました。
研究方法
患者さんの基本情報、移植情報、ECP情報を収集してECPの有効性と安全性を検討します。既にECP治療を開始され、同意が得られた場合には、同意取得前のECPに関する情報も収集して解析に用います。
解析結果は学会発表、学術論文として公表いたします。
個人情報の保護
この研究で得た情報は厳重に管理され、学術目的のみで利用されます。従って、学会発表や論文から個人が特定される恐れはありません。本研究参加者以外の第三者に個人情報が流出することもありません。各患者さんのプライバシーは厳重に保護されますのでご安心ください。
利益相反
私共の研究に関して、個人や会社との利益相反はありません。
お問い合わせ
研究への参加を拒否される場合は、当院の下記担当者までご連絡ください。
当院における連絡先:神鋼記念病院 血液内科/血液病センター
〒651-0072 神戸市中央区脇浜町1丁目4-47
Tel: 078-261-6711 Fax: 078-261-6726
血液内科 常峰 紘子
血液培養よりクロストリジウムが分離されたの患者さんおよびご家族へ
【過去の治療データを調査研究への使用のお願い】
神鋼記念病院血液内科では「当院におけるクロストリジウム菌血症の臨床的検討」という臨床研究を行っております。この研究は、2015年から2024年までの10年間に発熱などの症状で当院を受診された患者さんより採取された血液培養からクロストリジウム属の菌種が分離された患者さんの臨床的特徴を後方視的に調べることを主な目的としています。
以下の内容を確認してください。
○この調査研究は神鋼記念病院倫理委員会で審査され、病院長の承認を受けて行われます。研究期間は以下のとおりです。
調査対象期間 :2015年1月1日 ~ 2024年12月31日まで
データ収集期間:倫理委員会承認後 ~ 2025年11月30日
○今回の調査研究の対象は患者さんの生年月日、年齢、性別、既往歴、合併症、内服薬歴、抗生剤投与歴 等
・画像診断
頸胸腹部CT、頭部MRI、心臓・腹部超音波検査、胸部単純X線 等
・臨床検査
血液学的検査、血液生化学検査、細菌学的検査 等です。
○過去のデータを使用する研究であり、新たな検査や費用が生じることはなく、また、
データを使用させていただいた患者さんのご家族への謝礼等もありません。
○使用するデータは、個人が特定されないよう匿名化を行い、個人情報に関しては厳重に管理します。
○調査研究の成果は、学会や科学専門誌などの発表に使用される場合がありますが、名前など個人を特定するような情報が公表されることはなく、個人情報は守られます。
○調査研究の結果、特許などの知的財産が生じる可能性もございますが、その権利は神鋼記念病院に帰属し、あなたには帰属しません。
○この調査研究は、神鋼記念病院血液内科の研究費で行っており、特定の企業・団体等からの支援を受けて行われるものではなく、利益相反状態にはありません。
もし、今回のデータ使用について同意をいただけない場合には、2025年5月31日までに、お手数ですが下記の問い合わせ先まで連絡ください。
また、同意の有無が今後の治療などに影響することはございません。
【問い合わせ先】
神鋼記念病院 血液内科
研究責任者:有馬 靖佳
分担研究者:田中 康博
TEL:078-261-6711㈹
FCM(フローサイトメーター)検査と臨床検査所見の症例検討
当院に血液疾患等で入院された患者さん・ご家族様へ
症例検討へのご協力のお願い
当院では、以下の症例検討を実施しております。この検討は、日常診療で得られた以下の診療情報を他の医療従事者との情報共有を図るためのものです。検討のために、新たな検査などは行いません。この案内をお読みになり、ご自身またはご家族がこの症例検討の対象者にあたると思われる方で、ご質問がある場合、またはこの検討に診療情報を使ってほしくないとのご意思がある場合は、遠慮なく下記の担当者までご連絡ください。ただし、すでに検討を終了し、症例報告後の場合は、報告データから情報を削除できない場合がありますので、ご了承ください。
対象となる方
2024年4月1日から2024年10月31日に、当院にて血液疾患等の診断で入院された患者さんの内、FCM検査を受けられた患者さんに対し、以下の検討を行っています。
検討の目的
血液疾患等の患者さんに行うFCM検査にて得られる所見と、他の臨床検査や病理学的検査にて得られた診断所見とを比較検討し、より有用で精度高い診断に繋がるように、他の医療従事者と診断に関しての情報共有を図ることを目的としています。
利用する診療情報
- 年齢、性別
- 内科的背景、臨床症状
- 診療録、レントゲン等の画像情報、血液検査、病理検査などの検査結果
- 治療に用いた薬剤
- 発症時期
- 治療後の転帰
検討期間
検討許可日より2025年5月11日まで
個人情報の取り扱い
お名前、住所などの個人を特定する情報につきましては厳重に管理を行い、学会や学術雑誌等で公表する際には、個人が特定できないような形で使用いたします。
問合せ先
総合医学研究センター 担当技師 厨子 佑里子
電話 078-261-6711(代表)
神鋼記念病院における下部消化管出血の特徴及び治療成績の検討
神鋼記念病院の患者さんへ
2024年10月 神鋼記念病院消化器内科
1.研究の目的・意義
近年の高齢化などに伴い、本邦における憩室出血や虚血性腸炎などの下部消化管出血を来す疾患は増加傾向にあり、その治療法は、現在も研究されつつある分野です。そこで、当院における下部消化管出血を来された患者様に最適な治療方針を確立させるために、その症状に関連する疾患の背景や治療成績に関して検討いたします。
2.情報の取得期間
2021年11月から2031年8月31日の間に当院で下部消化管出血として入院された患者様を対象とします。
3.診療情報の項目
治療を受けられた患者様の臨床情報(年齢、身体所見、検査結果、入院前後の情報、画像・内視鏡所見、経過観察期間、転帰)について、診療録をもとに匿名化した状態で、解析に用います。
4.解析結果は学会発表、論文として公表いたします。
5.個人情報の保護
この研究で得た情報は厳重に管理され、学術目的のみで利用されます。従って、学会発表や論文から個人が特定される恐れはありません。本研究参加者以外の第三者に個人情報が流出することもありません。各患者さんのプライバシーは厳重に保護されますのでご安心ください。
6. 試料・情報の保管および破棄の方法
本研究では生体試料の採取は行わない。本研究で収集した情報は、研究の中止または研究終了後当該論文などの発表後20年間保存し、その後は個人情報に十分注意して破棄する。保管する資料・情報からは個人情報を削除し、連結不可能匿名化して保管する。保管場所はカルテおよび院内共有フォルダ内で管理する。
7.利益相反
私共の研究に関して、個人や会社との利益相反はありません。
8.研究への参加を拒否される場合は、当院の下記担当者までご連絡ください。
当院における連絡先
神鋼記念病院 消化器内科
〒651-0072 神戸市中央区脇浜町1丁目4-47 Tel: 078-261-6711, FAX: 078-261-6726
消化器内科: 塩 せいじ
ブリナツモマブ治療後に同種造血幹細胞移植を施行した再発・難治性B 細胞性急性リンパ性白血病の臨床アウトカム
臨床研究に関する情報および臨床研究に対するご協力のお願い
現在、神鋼記念病院と共同研究機関では、以前に「造血細胞移植および細胞治療の全国調査」のご協力者からいただいた診療情報等を使って、下記の研究課題を新たに実施しています。
この新たな研究課題の詳細についてお知りになりたい方は、下欄の研究内容の問い合わせ担当者まで直接お問い合わせください。なお、この新たな研究課題の研究対象者に該当すると思われる方の中で、ご自身の診療情報等を「この研究課題に対しては利用・提供して欲しくない」と思われた場合にも、下欄の研究内容の問い合わせ担当者までお申し出いただければ本研究での情報の利用又は提供を停止致します。その場合でも患者さんに不利益が生じることはありません。
研究課題名
ブリナツモマブ治療後に同種造血幹細胞移植を施行した再発・難治性B 細胞性急性リンパ性白血病の臨床アウトカム:
日本における造血細胞移植登録一元管理プログラム(TRUMP®)レジストリデータ及びその二次調査による後方視的観察研究 (研究略称:CORBLIN-T)
研究対象者
日本造血・免疫細胞療法学会及び日本造血細胞移植データセンターが実施している「造血細胞移植および細胞治療の全国調査」への協力に同意された患者さんのうち、2013年1月から2015年5月、もしくは2019年1月から2020年12月の間に東京女子医科大学血液内科又は共同研究機関にて、同種造血幹細胞移植(allo-HSCT)が施行されたB細胞性急性リンパ性白血病患者だった方。
情報の利用目的
(遺伝子解析研究:無)
研究目的は、研究対象の患者さんにおいてブリナツモマブ治療後、最初の移植施行後の安全性と有効性に関する臨床的結果を調べることです。
情報の利用方法
(主な提供方法:郵送・宅配,電子的配信)
造血幹細胞移植の実施時に「全国調査」の参加について研究機関で同意説明を行い、移植後から日本造血細胞移植データセンターに情報が提供されます。「全国調査」で日本造血細胞移植データセンターに集められた情報のうち、本研究の対象患者さんの情報を日本造血細胞移植データセンターが抽出します。また本研究の対象患者さんの追加移植情報が日本造血細胞移植データセンターに提供されます。これら2つの情報を用いて、日本造血細胞移植データセンターは本研究の対象患者さんの診療情報を解析し、ブリナツモナブで治療を受けた患者さんの移植施行後の安全性と有効性を検討します。
日本造血細胞移植データセンターは本研究の解析用データセットを作成し、東京女子医科大学病院と国立成育医療研究センターの研究責任者に対し、下記の診療情報等の取扱い方法を遵守して提供します。
本研究はアムジェン株式会社が研究実施のための資金を提供する産学協同研究ですが、研究計画は研究代表者および共同研究者が策定しています。アムジェン株式会社は研究で収集された診療情報は利用しません。個人が特定されない状態にされた本研究の集計解析結果を利用する予定です。
利用している診療情報等の項目
移植前のブリナツモマブ投与情報と同種造血幹細胞移植に関わる診療情報:- 患者さんの移植診療情報(年齢、性別、移植時病期、HCT-CI スコア、移植前のperformance status、診断から移植までの期間、移植前処置、前化学療法レジメン数、抗ヒトT 細胞グロブリン使用の有無、移植片対宿主病(GVHD)予防法)
- ドナーさんの診療情報(ドナー・細胞種類、ヒト白血球抗原適合度、患者・ドナーの性別の不一致)
- 患者さんの移植後経過(再発の有無、生存状況、移植後の疾患の状況、急性GVHD の有無、慢性GVHD の有無、好中球数500/μL 以上の到達日、血小板数2 万/μL 以上の到達日、サイトメガロウイルス感染症の有無、二次性生着不全の有無、類洞閉塞症候群/肝中心静脈閉塞症の有無、非感染症肺合併症の有無、移植後リンパ増殖性疾患の有無)
情報を利用又は提供を開始する予定日
本研究の倫理審査委員会承認後から2025 年11 月30 日を予定しています。
共同研究機関及び研究責任者、情報を利用する者の範囲
- 東京女子医科大学血液内科 講師 篠原 明仁(研究代表機関・研究代表者)
- 国立成育医療研究センター 小児がんセンター 移植・細胞治療科 診療部長 坂口 大俊(研究事務局)
- 一般社団法人 日本造血細胞移植データセンター センター長 熱田 由子
- 全国の造血幹細胞移植実施機関(施設名は日本造血細胞移植データセンターホームページで公表)
- アムジェン株式会社 メディカルアフェアーズ本部 メディカル・サイエンス・リエゾン 松島 敏志
1〜4の共同研究機関および関係者が[利用している診療情報等の項目]で示した情報を利用し解析を行います。
得られた解析結果は1〜5の共同研究機関および関係者が利用します。
国外への情報の提供は予定していません。
情報の管理について責任を有する者の氏名又は名称
- 東京女子医科大学血液内科 講師 篠原 明仁
- 国立成育医療研究センター 小児がんセンター 移植・細胞治療科 診療部長 坂口 大俊
- 一般社団法人 日本造血細胞移植データセンター 理事長 岡本 真一郎
- 全国の造血幹細胞移植実施機関(責任者は日本造血細胞移植データセンターホームページで公表)
- アムジェン株式会社 メディカルアフェアーズ本部 メディカル・サイエンス・リエゾン 松島 敏志
研究実施期間
倫理審査委員会承認日から2027年12月31日(論文の公表)まで
この研究での診療情報等の取扱い
本研究の情報は個人情報保護法及び文部科学省・厚生労働省・経済産業省が定める「人を対象とする生命科学・医学系研究に関する倫理指針」の要件を満たした上で提供します。東京女子医科大学倫理審査委員会の承認を受けた研究計画書に従い、お預かりした診療情報等の氏名、現住所、電話番号、生年月日等の情報は含めず、患者さん及びドナーさんのプライバシー保護に配慮をした上で取り扱っています。
研究責任者、研究機関の長、および研究内容の問い合わせ担当者
研究責任者: 神鋼記念病院血液内科 常峰 紘子
研究機関の長: 神鋼記念病院長 東山 洋
研究内容の問い合わせ担当者: 神鋼記念病院血液内科 常峰 紘子
電話:078-261-6711(応対可能時間:9時~17時)
当院で生じた免疫チェクポイント阻害剤による消化器有害事象の特徴及び対応についての検討
神鋼記念病院の患者さんへ
2024年10月 神鋼記念病院消化器内科
1.研究の目的・意義
近年の癌治療において免疫チェックポイント阻害剤の使用は増加傾向にあり、それに伴う有害事象は現在も研究されつつある分野です。そこで、免疫チェックポイント阻害剤における有害事象に対しての最適な対応を確立させるために、その症状に関連する疾患の背景や治療成績に関して検討いたします。
2.情報の取得期間
2018年4月から2030年3月31日の間に当院で癌薬物療法として免疫チェックポイント阻害剤を使用した患者様を対象とします。
3.診療情報の項目
治療を受けられた患者様の臨床情報(年齢、身体所見、検査結果、入院前後の情報、治療内容、画像・内視鏡所見、経過観察期間、転帰等)について、診療録をもとに匿名化した状態で、解析に用います。
4.解析結果は学会発表、論文として公表いたします。
5.個人情報の保護
この研究で得た情報は厳重に管理され、学術目的のみで利用されます。従って、学会発表や論文から個人が特定される恐れはありません。本研究参加者以外の第三者に個人情報が流出することもありません。各患者さんのプライバシーは厳重に保護されますのでご安心ください。
6.資料・情報の保管および破棄の方法
データについては外部からアクセスすることができない高セキュリティ下のサーバーで保存いたします。保存期間は研究終了後5年間とし、保存期間終了時に個人情報に十分注意してデータを破棄いたします。
7.利益相反
私共の研究に関して、個人や会社との利益相反はありません。
8.研究への参加を拒否される場合は、当院の下記担当者までご連絡ください。
神鋼記念病院 消化器内科: 塩 せいじ
神戸市中央区脇浜町1丁目4-47 Tel: 078-261-6711, FAX: 078-261-6726
筋炎特異自己抗体、筋炎関連自己抗体を有する間質性肺炎の後方視的観察研究
研究課題名
筋炎特異自己抗体、筋炎関連自己抗体を有する間質性肺炎の後方視的観察研究
本件は「オプトアウト」すなわち、同意不要であった既存データを用いた研究において、「自分のデータは使わないでほしい」という、患者さんの拒否の機会を確保するため、研究の公開をホームページ上で行っているものです。 今回の研究に該当されることが予想され、「自分のデータは使わないでほしい」と希望される方はご本人・ご家族より当院に手紙、メール、お電話もしくはファックスなどにてその旨ご連絡ください。
神鋼記念病院で採血検査を施行し筋炎特異自己抗体、筋炎関連自己抗体を認めた間質性肺炎の患者さんへ
実施する臨床研究
該当する患者さんの診療経過について調査研究を実施しております。この研究は「観察研究」と呼ばれるもので、 通常の診療で得られた記録をまとめることによって行います。以下の点をご理解いただき、ご協力いただきますようお願い申し上げます。
この研究の意義、目的、および方法
多発性筋炎/皮膚筋炎(PM/DM)などの炎症性筋疾患は間質性肺疾患(ILD)を合併することが多く、また筋炎関連自己抗体の種類により臨床経過が異なることが報告されています。 アミノアシルtRNA合成酵素に対する自己抗体である抗ARS抗体は、筋炎、発熱、多関節炎、間質性肺炎、Raynaud現象、機械工の手といった抗ARS抗体症候群と呼ばれる臨床症状を呈する場合があり、 現在8種類(①抗Jo-1抗体②抗EJ抗体③抗PL-7抗体④抗PL-12抗体⑤抗KS抗体⑥抗OJ抗体⑦抗Zo抗体⑧抗Ha抗体)の抗体が同定されています。 抗ARS抗体以外では抗MDA5抗体が重要で、 陽性例では筋症状は乏しいが数日から数週間の経過で急速に進行するILDを高頻度に合併し重症化頻度が高い事が知られています。2020年にPM/DMに合併するILDに関して、日本呼吸器学会と日本リウマチ学会の共同で作成された「膠原病に伴う間質性肺疾患の診断・治療指針」において、治療アルゴリズム案が提案され、 身体所見、画像所見で急性/亜急性、慢性、に分類し、特にILDが急速進行性の例では抗MDA-5抗体陽性を想定してステロイドパルス療法を含む高用量PSLにカルシニューリン阻害薬、シクロホスファミド間欠大量静注療法を初期より用いる3剤併用療法を行うことが推奨されています。上記以外にも筋炎特異自己抗体として抗SRP抗体、抗Mi-2抗体、抗TIF-1γ抗体、抗NXP-2抗体、抗HMGCR抗体が、 筋炎関連自己抗体として抗SS-A/Ro-52抗体、 抗Ku抗体、 抗U1RNP抗体、 抗PM-Scl抗体が挙げられ、 それぞれの自己抗体に対応する臨床的特徴があるため、 筋炎の分類、検査方針、治療方針の決定と予後予測に自己抗体の測定は有用と考えられています。一方で、 各抗体ごとの治療薬に対する質の高いエビデンスはまだありません。 とりわけ筋炎を伴わない筋炎特異的・関連自己抗体を伴うILDについては報告例が少なく、臨床経過と予後についてはいまだよく分かっていません。 治療方針もやはり定まったものがなく、ILDの経過中に皮膚筋炎を発症する症例もみられるため、 画像パターンや組織所見、臨床経過を鑑みて皮膚筋炎を伴うILDに準じて治療されることが多いです。筋炎特異抗体、筋炎関連抗体を有する間質性肺炎患者の各抗体による臨床像、治療反応性、予後の違いを明らかにするために本研究を実施します。2010/8/1以降に当院で抗Jo-1抗体 (LSI)、抗ARS抗体 (LSI)、EUROLINE(筋炎関連抗体セット)、 A-cube(DM/PM関連自己抗体セット)を測定し、いずれかで筋炎特異自己抗体あるいは筋炎関連自己抗体を検出した患者さんの内、間質性肺炎を伴う方を対象とします。 診療録から年齢、 性別、 喫煙歴、 併存疾患、 画像データ、 血液検査結果、 生理検査結果、 内視鏡検査結果等を後方視的に調査し、 解析します。
この研究による医学上の貢献と予測
日常臨床で得られる情報を通して、筋炎特異自己抗体、筋炎関連自己抗体を有する間質性肺炎の患者さんに、 より適切な診療を届けられる方法を検討します。
この研究による患者さんの不利益および危険性
患者さんの診療情報を分析する研究であり、プライバシーも厳重に保護されますので、患者さんに不利益や危険性はありません。
費用や追加の検査
通常の保険診療による画像診断情報と臨床情報の収集と分析ですので、患者さんに余分な費用を負担してもらうことはありません。また、検査方法の変更や追加検査もありません。
個人情報の保護
この研究で得た情報は厳重に管理され、学術目的のみで利用されます。 研究結果は主として統計として処理・解析され発表されるため、個人を特定できることはありません。研究結果の発表に際して、一部の患者さんの臨床情報が参考所見として呈示される可能性がありますが、匿名化されていますので、個人を特定できることはありません。 本研究参加者以外の第三者に流出することもありません。以上のように、患者さんのプライバシーは厳重に保護されますのでご安心ください。
ご協力の拒否について
この研究にご自分のデータが使用されることを拒否される場合は、担当医もしくは下記の問い合わせ先に連絡下さい。 たとえ、協力を拒否されても、今後の診療の不利益になることはありません。しかし、拒否のお申し出のあった時点で、 既に研究結果が論文などで公表されていた場合には、 研究結果を破棄できないことがあります。 この場合でも個人が特定されることはありませんので個人情報は保護されます。
研究責任者
神鋼記念病院 呼吸器内科 門田 和也
当院における連絡先
神鋼記念病院 呼吸器内科 門田 和也
〒651-0072 神戸市中央区脇浜町1丁目4-47
TEL:078-261-6711 ・ FAX:078-261-6931
神鋼記念病院におけるロボット支援腹腔鏡下腎部分切除術(RAPN)の治療成績、播種再発を来した症例の検討
神鋼記念病院泌尿器科の患者さんへ
1.研究の目的・意義
小径腎細胞癌に対するロボット支援腹腔鏡下腎部分切除術(RAPN)は標準的な治療方法として確立されており、本邦でも広く行われています。しかし、周術期の成績や腫瘍学的治療成績について検討し、さらなる術式改良などにつなげる必要性があります。そこで当院で小径腎細胞癌に対するRAPNを施行された患者様の周術期成績や術後腎機能および腫瘍学的治療成績を検討いたします。
2.情報の取得期間
2017年12月1日から2024年8月31日の間に当院で小径腎細胞癌に対するRAPNを受けられた患者様を対象とします。
3.診療情報の項目
手術を受けられた患者様の臨床情報(年齢、身体所見、検査結果、術前の情報、画像所見、経過観察期間、転帰)について、診療録をもとに匿名化した状態で、解析に用います。
4.解析結果は学会発表、論文として公表いたします。
5.個人情報の保護
この研究で得た情報は厳重に管理され、学術目的のみで利用されます。従って、学会発表や論文から個人が特定される恐れはありません。本研究参加者以外の第三者に個人情報が流出することもありません。各患者さんのプライバシーは厳重に保護されますのでご安心ください。
6.利益相反
私共の研究に関して、個人や会社との利益相反はありません。
7.研究への参加を拒否される場合は、当院の下記担当者までご連絡ください。
当院における連絡先
神鋼記念病院 泌尿器科
〒651-0072 神戸市中央区脇浜町1丁目4-47 Tel: 078-261-6711, FAX: 078-261-6726
泌尿器科: 坂田 宏行
術前治療後に切除し病理学的完全奏効(pCR)であった膵癌症例における臨床病理学的意義の検討
1.研究の名称
術前治療後に切除し病理学的完全奏効(pCR)であった膵癌症例における臨床病理学的意義の検討
2.倫理審査と許可
京都大学大学院医学研究科・医学部及び医学部附属病院 医の倫理委員会の審査を受け、研究機関の長の許可を受けて実施しています。
3.研究機関の名称・研究責任者の氏名
研究代表機関
京都大学大学院医学研究科 肝胆膵・移植外科 教授 波多野悦朗
共同研究機関
- 大原記念倉敷中央医療機構 倉敷中央病院 外科部長 増井俊彦
- 地方独立行政法人 京都市立病院機構 京都市立病院 総合外科副部長 奥田雄紀浩
- 金沢大学附属病院 肝胆膵・移植外科教授 八木真太郎
- 小倉記念病院 外科副院長 藤川貴久
- 滋賀県立総合病院 外科長 山中健也
- 医学研究所北野病院 消化器外科副部長 井口公太
- 三菱京都病院 消化器外科医師 戸田怜
- 地方独立行政法人神戸市民病院機構神戸市立西神戸医療センター 消化器外科医長 畑俊行
- 日本赤十字社 大津赤十字病院 外科部医長 北口和彦
- 京都桂病院 消化器センター・外科医長 岡村裕輔
- 大阪赤十字病院 消化器外科副院長 森章
- 神鋼記念病院 消化器外科医長 小松原隆司
- 福井赤十字病院 外科部長 土居幸司
- 大阪府済生会野江病院 消化器外科副部長 壷井邦彦
- 天理よろづ相談所病院 外科部長 待本貴文
- 兵庫県立尼崎総合医療センター 消化器外科部長 北村好史
- 日本赤十字社和歌山医療センター 消化器外科主任部長 安近健太郎
- 神戸市立医療センター中央市民病院 外科医長 成田匡大
4.研究の目的・意義
本研究は、術前治療で病理学的完全奏功(pCR)となった膵癌症例の腫瘍学的予後と臨床病理学的特徴を明らかにすることを目的としています。本研究により、pCRを得やすい術前治療の内容や治療期間を明らかにすることができます。
5.研究実施期間
研究機関の長の実施許可日から2026年6月30日まで
6.対象となる試料・情報の取得期間
京都大学医学部附属病院および共同研究機関において、2013年1月1日から2022年9月30日までに根治手術が施行された膵癌患者さんのうち、術前治療を実施された患者さん
7.試料・情報の利用目的・利用方法
術前治療後に根治切除を実施された患者さんを臨床データや手術データを用い、pCRを得られた患者さんの情報とpCRを得られなかった患者さんの情報を比較し統計解析を行います。
8.利用または提供する試料・情報の項目
患者さんの背景・治療前情報、術前治療後・手術前情報、手術情報、病理学的情報、予後情報を利用します。
9.利用または提供を開始する予定日
各研究機関の長の実施許可日以降に利用します。
10.試料・情報の管理について責任を有する者の氏名または名称
京都大学大学院医学研究科 肝胆膵・移植外科 講師 長井和之
11.研究対象者またはその代理人の求めに応じて、研究対象者が識別される試料・情報の利用または他の研究機関への提供を停止すること及びその方法
ご自身の試料・情報を研究に利用されたくない方は、連絡先までその旨お知らせ頂ければ、解析対象から削除します。
12.他の研究対象者等の個人情報および知的財産の保護等に支障がない範囲内での研究に関する資料の入手・閲覧する方法
他の研究対象者等の個人情報及び知的財産に支障がない範囲で研究に関する資料の入手・閲覧が可能です。希望される方は、問合せ窓口までお知らせください。
13.研究資金・利益相反
本研究に要する費用は、公益財団法人膵臓病研究財団からの寄附金にて負担します。 研究代表機関の研究者の利益相反については、京都大学利益相反ポリシー、京都大学利益相反マネジメント規程に従い、京都大学臨床研究利益相反審査委員会において適切に審査されています。共同研究機関においても各機関の規程に従い審査されています。
14.研究対象者等からの相談への対応
- 研究課題ごとの相談窓口
京都大学大学院医学研究科 肝胆膵・移植外科 講師 長井和之
〒606-8507 京都府京都市聖護院川原町54
TEL: 075-751-3242 FAX:075-751-4263
E-mail: kaznagai@kuhp.kyoto-u.ac.jp - 各研究機関における相談等窓口
京都大学医学部附属病院 臨床研究相談窓口
TEL:075-751-4748
E-mail:ctsodan@kuhp.kyoto-u.ac.jp - 当院の相談等窓口
神鋼記念病院 消化器外科 医長 小松原隆司
〒651-0072兵庫県神戸市中央区脇浜町1-4-47
TEL: 078-261-6711 FAX:078-261-6726
80歳以上の高齢鼠径ヘルニア患者に対する至適手術治療の検討
:京都大学外科関連多機関共同コホート研究
2019年1月1日から2023年12月31日までに当院(神鋼記念病院)で鼠径ヘルニアに対して手術を受けられた患者さんへ
1.研究の名称
80歳以上の高齢鼠径ヘルニア患者に対する至適手術治療の検討
:京都大学外科関連多機関共同コホート研究
2.倫理審査と許可
京都大学大学院医学研究科・医学部及び医学部附属病院 医の倫理委員会の審査を受け、当院での倫理委員会の許可も受けて実施しています。
3.研究の目的・意義
この研究は、80歳以上の高齢の鼠径ヘルニア患者さんに対するより良い術式と麻酔の方法を評価し、日常診療における適切な治療選択肢を明らかにします。
4.研究実施期間
研究期間は研究機関の長の実施許可日から2027年3月31日までを予定しています。
5.対象となる試料・情報の取得期間
当院消化器外科で2019年1月1日から2023年12月31日までに鼠径ヘルニアに対して腹腔鏡下手術もしくは鼠径部切開法を受けられた80歳以上の患者さんが対象となります。
6.試料・情報の利用目的・利用方法
カルテに保存されているデータを後方視的に収集します。データは、各機関において個人を特定できる情報を削除し、研究代表機関である京都大学に集約されます。患者さんの個人情報を公開することはありません。
7.利用または提供する試料・情報の項目
利用する情報はカルテに保存されているデータ(年齢、性別、疾患名、手術の術式、手術前後の治療、手術の成績など)です。
8.利用または提供を開始する予定日
研究機関の長の実施許可日から
9.試料・情報の管理について責任を有する者の氏名または名称
京都大学医学部附属病院消化管外科 教授 小濵和貴
10.研究対象者またはその代理人の求めに応じて、研究対象者が識別される試料・情報の利用または他の研究機関への提供を停止すること及びその方法
ご自身の試料・情報を研究に利用されたくない方は、連絡先までその旨お知らせ頂ければ、解析対象から削除します。
11.他の研究対象者等の個人情報および知的財産の保護等に支障がない範囲内での研究に関する資料の入手・閲覧する方法
他の研究対象者等の個人情報及び知的財産に支障がない範囲で研究に関する資料の入手・閲覧が可能です。希望される方は、相談窓口までお知らせください。
12.研究資金・利益相反
この研究は消化管外科運営交付金を資金源とし、利益相反については「京都大学利益相反ポリシー」「京都大学利益相反マネジメント」に従い「京都大学臨床研究利益相反審査委員会」において適切に審査しています。
13.研究対象者等からの相談への対応
1)研究課題ごとの相談窓口
京都大学医学部附属病院消化管外科医局
水野良祐
〒606-8507 京都市左京区聖護院川原町54
TEL:075-366-7595
2)京都大学の相談窓口
京都大学医学部附属病院臨床研究相談窓口
TEL:075-751-4748
E-mail:ctsodan@kuhp.kyoto-u.ac.jp
3)当院の相談窓口
神鋼記念病院 消化器外科
谷川優麻
〒651-0072 神戸市中央区脇浜町1丁目4-47
TEL:078-261-6711
14.研究機関及び共同研究機関の名称・研究責任者の氏名
1)研究代表機関 研究責任者:
京都大学医学部附属病院消化管外科 教授 小濵和貴
2)共同研究機関 研究責任者(施設50音順):
- 医学研究所北野病院 消化器外科 河合隆之
- 宇治徳洲会病院 外科 島田明
- 大阪赤十字病院 消化器外科 西田和樹
- 大津赤十字病院 外科 安宅亮
- 大原記念倉敷中央医療機構 倉敷中央病院 外科 武田直人
- 関西電力病院 消化器外科 増田健人
- 京都市立病院機構 京都市立病院 総合外科 西川裕太
- 神戸市立医療センター中央市民病院 外科・移植外科 成田匡大
- 神戸市立医療センター西市民病院 消化器外科 本間周作
- 神戸市立西神戸医療センター 外科・消化器外科 土佐明誠
- 公立豊岡病院組合立 豊岡病院 消化器外科 河原林卓馬
- 小倉記念病院 外科 長田圭司
- 国立病院機構 京都医療センター 外科 末永尚浩
- 国立病院機構 姫路医療センター 消化器外科 守山雅晃
- 国家公務員共済組合連合会 枚方公済病院 外科 増井秀行
- 滋賀県立総合病院 外科 参島祐介
- 神鋼記念病院 消化器外科 谷川優麻
- 杉田玄白記念公立小浜病院 外科・消化器外科 平山楓
- 高松赤十字病院 消化器外科 森本智紀
- 天理よろづ相談所病院 消化器外科 岩崎雄太
- 彦根市立病院 消化器外科 佐々木悠大
- 福井赤十字病院 外科 坂本裕生
- 兵庫県立尼崎総合医療センター 消化器外科 谷野敬輔
- 洛和会音羽病院 外科 花田圭太
閉経前ホルモン受容体陽性乳癌の術後内分泌療法に関した後方視的研究
2024年1月11日 第1.1版
2024年2月1日 第1.2版
1.研究対象
研究許可日から2028年3月にかけて行われる研究です。術前・術後薬物療法の有無によらず、2008年から2017年までの手術を受けたホルモン受容体陽性HER2陰性N0-1(術後症例は病理学的に、術前化学療法症例は臨床的な腋窩リンパ節転移の個数を含む)の閉経前乳がん(または閉経状態が不明な場合は50歳未満の患者さん)を対象とします。
2.研究の目的
閉経前ホルモン受容体陽性乳がんにおける術後症例の予後について検討することを目的としています。
3.研究の方法
各施設で本研究に参加された患者さんの治療前後及び治療中の状況、疾患の経過を含む、以下の情報を収集いたします。これらの情報は診療録(各種の検査結果、診療ために撮影された画像、及び提出された腫瘍組織の病理評価結果など、診療録の記載)から調査致します。
研究実施期間:研究許可日~2028年3月31日
□ 基本情報
年齢、性別、ホルモン受容体やHER2タンパク質等の発現状況、転移の有無
□ 患者さんの背景や疾患等に関する情報
身長、体重および全身状態等の背景情報、手術した乳がんと診断時に関連する情報(手術歴、病理評価など)、周術期の抗がん剤治療の治療歴、腫瘍に対する治療効果、放射線治療、手術の内容、術後内分泌療法の詳細と投与期間、再発の有無、再発場所、最終の転帰。
4.研究に用いる試料・情報の種類
臨床・病理学的項目:診断日、進行度、組織分類、治療歴、臨床経過など
カルテの情報を収集します。
5.外部への試料・情報の提供
個人が特定できない状態で情報を収集します。
研究対象者には研究用番号を付し匿名化を行います。研究用番号と個人識別情報(氏名、カルテ番号)を結ぶ対応表は、症例集積を行う各機関の研究責任者が管理し、容易に個人を特定できないように匿名化した状態のデータのみを収集します。各研究者は、研究代表機関(国立がん研究センター中央病院)へ患者情報の提供を行います。収集されたデータは特定の関係者以外がアクセスできない状態で行います。研究結果の報告、発表に関しては個人を特定される形では公表しません。本研究で用いた試料・情報を国内外の機関で実施する将来の医学的研究のために、研究終了後も大切に保管させていただきます。新たな研究に用いる際には、国内外の規制に則り、あらためて研究計画書を作成して研究倫理審査委員会の承認や研究機関の長の許可を受ける等、適正な手続を踏んだ上で行います。なお、新たな研究の概要・研究機関については、新たな研究に関わる機関(試料・情報の授受を行う機関すべて)公式ホームページ等にて情報公開いたします。
・国立がん研究センターが参加する研究の公開情報については国立がん研究センターの公式ホームページより確認することができます。
https://www.ncc.go.jp/jp
6.研究組織
研究代表機関
| 研究機関名 | 研究代表者氏名 | 研究機関の長の氏名 |
| 国立がん研究センター中央病院 | 下井辰徳 | 中釜斉 |
共同研究機関
- 国立がん研究センター中央病院を含む国内外約10施設
各機関の研究責任者
- 石川 孝
東京医科大学病院 乳腺科学分野 - 上野 直人
ハワイ大学がんセンター
University of Hawaiʻi Cancer Center - 鶴谷 純司
昭和大学病院 先端がん治療研究臨床センター - 成井 一隆
横浜市立大学附属市民総合医療センター 乳腺・甲状腺外科 - 松本 光史
兵庫県立がんセンター 腫瘍内科 - 山田 顕光
横浜市立大学附属病院 乳腺外科 - 喜多 久美子
聖路加国際病院 乳腺外科 - 中村 力也
千葉県がんセンター 乳腺外科 - 山神 和彦
神鋼記念病院 乳腺センター
統計解析責任者
- 田栗 正隆
折原 隼一郎(共同研究者)
東京医科大学 医療データサイエンス分野
7.お問い合わせ先
本研究に関するご質問等がありましたら下記の連絡先までお問い合わせ下さい。ご希望があれば、他の研究対象者の個人情報及び知的財産の保護に支障がない範囲内で、研究計画書及び関連資料を閲覧することが出来ますのでお申出下さい。
また、試料・情報が当該研究に用いられることについて患者さんにご了承いただけない場合には研究対象としませんので、下記の連絡先までお申出ください。その場合でも患者さんに不利益が生じることはありません。
- 照会先および研究への利用を拒否する場合の連絡先:
研究事務局,研究代表者:
国立がん研究センター中央病院 腫瘍内科 下井 辰徳
〒104-0045
東京都中央区築地5-1-1
TEL: 03-3542-2511 - 研究機関
神鋼記念病院 乳腺センター 山神 和彦
〒651-0072
神戸市中央区脇浜町1-4-47
TEL: 078-261-6711
本研究に関する苦情、相談、あるいはお問い合わせについては、以下の相談窓口を設置しています。ご相談したいことがある場合にはご利用ください。
- 【連絡先】
国立がん研究センター中央病院 腫瘍内科 下井 辰徳
〒104-0045
東京都中央区築地5-1-1
TEL: 03-3542-2511
バンコマイシンの1点採血と2点採血のAUCの比較
神鋼記念病院に入院歴のある患者さん、または現在入院中及び通院中の患者さんへ
実施する臨床研究
当院では、バンコマイシン(VCM)を使用している患者さんに関する臨床研究を実施しております。この研究は、「観察研究」と呼ばれるもので、通常の診療で得られた記録をまとめることによって行います。
以下の点をご理解いただき、ご協力いただきますようお願い申し上げます。
研究目的・意義
VCMは重症感染症などに使用される抗菌薬で、投与量によって腎障害などの副作用を発症することがあります。そのため学会では、血中濃度を2回(点滴投与前と投与終了後)測定することを推奨しており、当院でもより安全に使用するため全例2回採血を行い、投与量を調整しています。しかし、全例に2回採血を続けていくことは、患者さんの負担にもつながるため、2回採血ではなく1回の採血でも問題がない要因を検索していきたいと考えております。
研究方法
当院においてVCMを使用し血中濃度を2回測定した入院患者さんを対象に、患者情報などを評価します。
電子カルテに記載のある診療録を利用し、検討を行います。
1)患者基本情報:年齢、性別、主病名、起因菌、内服・注射内容
2)身体所見:身長、体重、BMI
3)血液検査:アルブミン、AST、ALT、Scr、eGFR、Na、K
4)その他:VCMの血中濃度、1日投与回数、投与時間
研究成果の公表について
研究成果が学術目的のために論文や学会で公表されることがありますが、その場合には、患者さんを特定できる情報は利用しません。
研究へのデータ提供による不利益・危険性
患者さんの診療情報を分析する研究であり、プライバシーも厳重に保護されますので、患者さんに不利益や危険性はありません。また、追加の検査や余分な費用を負担していただくこともありません。
研究への参加とその撤回について
事例報告の発表にご協力いただくかどうかは、ご自身やご家族のお考えで、自由に決めていただきます。お断りになっても不利益を受けることはありません。ただし拒否のお申し出のあった時点ですでに研究結果が公表されていた場合は、完全に破棄できないことがあります。
個人情報の保護について
この研究で得た情報は神鋼記念病院院内サーバーに作成した管理用ファイルで厳重に管理され、学術目的のみで利用されます。検査結果や診療情報は統計として処理・解析されるため、個人を特定できることはありません。 本研究参加者以外の第三者に流出することもありません。尚、研究目的以外にデータを使用することはありません。
問い合わせ窓口
神鋼記念病院 診療技術部薬剤室
〒651-0072 神戸市中央区脇浜町1丁目4-47
TEL:078-261-6711・FAX:078-261-6726
主たる研究者 薬剤師 : 真砂 聖
研究責任者 薬剤師 : 依藤 健之介
当院のHoLEPの術式変更と術後尿失禁の検討
2024年11月28日より30日まで千葉県の幕張メッセ国際会議場で開催される第38回日本泌尿器内視鏡・ロボティクス学会総会で、当院泌尿器科山下真寿男が上記発表を行う予定です。
学会発表の意義
当院で前立腺肥大症に対するホルミウムレーザー前立腺核出術(HoLEP)を2010年1月より2024年3月までに行った患者さんの治療成績を使ったデータをまとめた結果となります。当初行なっていた核出方法と2022年6月以後に行なっている方法の術後尿失禁の成績を比較しました。改善された新しい手技は特に早期の尿失禁予防に優れていることが示唆されました。
プライバシー
患者さんの診療情報を分析する検討・発表であり、患者さんを特定できるような表現を用いませんのでプライバシーも厳重に保護されます。患者さんに不利益や危険は及びません。
個人情報の保護
この検討・発表で得た情報は厳重に管理され、学術目的のみで利用されます。研究結果は主として統計として処理・解析されるため、個人を特定することはありません。発表に際して、一部患者さんの画像が参考資料として呈示されることはありますが、画像は匿名化されているので、個人を特定することはできません。以上のように患者さんのプライバシーは厳重に保護されていますのでご安心ください。
ご協力の拒否について
当発表にご自分のデータが使用されることを拒否される場合は、当院泌尿器科山下真寿男もしくは下記の問い合わせ先にご連絡ください。たとえ、協力を拒否されても、今後の診療の不利益になることはありません。しかし、拒否の申し出があった時点で、すでに発表が終了していた場合には、データを削除できません。この場合でも個人が特定されることはありませんので個人情報は保護されます。
学会発表者
神鋼記念病院 泌尿器科 山下真寿男
共同発表者 中村稜、小笠原康貴、坂田宏行、結縁敬治
当院における連絡先
神鋼記念病院 泌尿器科 山下真寿男
〒651-0072神戸市中央区脇浜町1-4-47
TEL:078-261-6711・FAX:078-261-6726
原発性アルドステロン症における腹腔鏡下副腎摘除術後の高血圧治療成績についての検討
神鋼記念病院泌尿器科の患者さんへ
1.研究の目的・意義
原発性アルドステロン症に対する腹腔鏡下副腎摘除術は高血圧に対する標準的な治療方法として確立されており、本邦でも広く行われています。しかし、手術を施行されたすべての患者様の高血圧が完全に治癒するわけではなく、術後も降圧剤の内服が必要となる方が一定数存在されます。そこで当院で原発性アルドステロン症に対する腹腔鏡下副腎摘除術を施行された患者様の治癒率に関わる因子を検討致します。
2.情報の取得期間
2017年4月1日から2023年9月30日の間に当院で原発性アルドステロン症に対する腹腔鏡下副腎摘除術を受けられた患者様を対象とします。
3.診療情報の項目
手術を受けられた患者様の臨床情報(年齢、身体所見、検査結果、術前の情報、画像所見、経過観察期間、転帰)について、診療録をもとに匿名化した状態で、解析に用います。
4.解析結果は学会発表、論文として公表いたします。
5.個人情報の保護
この研究で得た情報は厳重に管理され、学術目的のみで利用されます。従って、学会発表や論文から個人が特定される恐れはありません。本研究参加者以外の第三者に個人情報が流出することもありません。各患者さんのプライバシーは厳重に保護されますのでご安心ください。
6.利益相反
私共の研究に関して、個人や会社との利益相反はありません。
7.研究への参加を拒否される場合は、当院の下記担当者までご連絡ください。
当院における連絡先: 神鋼記念病院 泌尿器科
〒651-0072 神戸市中央区脇浜町1丁目4-47 Tel: 078-261-6711, FAX: 078-261-6726
泌尿器科: 坂田 宏行
呼吸器疾患患者における将来の肺高血圧症発症の予測手法を確立するための後方視的検討
本件は「オプトアウト」すなわち,同意不要であった既存データを用いた研究において、「自分のデータは使わないでほしい」という、患者さんの拒否の機会を確保するため、研究の公開をホームページ上で行っているものです。 今回の研究に該当されることが予想され、「自分のデータは使わないでほしい」と希望される方はご本人・ご家族より当院に手紙、メール、お電話もしくはファックスなどにてその旨ご連絡ください。
神鋼記念病院に通院・入院し、呼吸器疾患があり精査のために右心カテーテルを受けたことのある患者さんへ
実施する臨床研究
呼吸器疾患があり肺高血圧症を有していないか右心カテーテル検査を受けたことがある患者さんの診療経過について調査研究を実施しております。この研究は「観察研究」と呼ばれるもので、 通常の診療で得られた記録をまとめることによって行います。以下の点をご理解いただき、ご協力いただきますようお願い申し上げます。
この研究の意義、目的、および方法
肺高血圧症は早期診断が困難な疾患ですが、呼吸器疾患にも合併することがあり、進行すると寿命に影響する疾患です。しかしながら、呼吸器疾患において将来肺高血圧を発症するかどうかを事前に予測する方法はあきらかとなっていません。呼吸器疾患の患者さんの診療経過を調査し、その方法を確立することは、より正確な予後の予測や、適切な治療介入につなげるために重要であると考えられます。本研究では呼吸器疾患をお持ちで肺高血圧症が疑われ右心カテーテル検査を施行された症例を対象として、これまでの患者背景情報、各種検査結果、治療経過などを調査し解析します。
この研究による医学上の貢献と予測
日常臨床で得られる情報を通して、呼吸器疾患の患者さんが肺高血圧を将来発症するかどうか予測する方法を見出します。
この研究による患者さんの不利益および危険性
患者さんの診療情報を分析する研究であり、プライバシーも厳重に保護されますので、患者さんに不利益や危険性はありません。
費用や追加の検査
通常の保険診療による画像診断情報と臨床情報の収集と分析ですので、患者さんに余分な費用を負担してもらうことはありません。また、検査方法の変更や追加検査もありません。
個人情報の保護
この研究で得た情報は厳重に管理され、学術目的のみで利用されます。 研究結果は主として統計として処理・解析され発表されるため、個人を特定できることはありません。研究結果の発表に際して、一部の患者さんの臨床情報が参考所見として呈示される可能性がありますが、匿名化されていますので、個人を特定できることはありません。 本研究参加者以外の第三者に流出することもありません。以上のように、患者さんのプライバシーは厳重に保護されますのでご安心ください。
ご協力の拒否について
この研究にご自分のデータが使用されることを拒否される場合は、担当医もしくは下記の問い合わせ先に連絡下さい。 たとえ、協力を拒否されても、今後の診療の不利益になることはありません。しかし、拒否のお申し出のあった時点で、 既に研究結果が論文などで公表されていた場合には、 研究結果を破棄できないことがあります。 この場合でも個人が特定されることはありませんので個人情報は保護されます。
研究責任者
神鋼記念病院 呼吸器内科 稲尾 崇
当院における連絡先
神鋼記念病院 呼吸器内科 稲尾 崇
〒651-0072 神戸市中央区脇浜町1丁目4-47
TEL:078-261-6711 ・ FAX:078-261-6931
関節リウマチ患者における生物学的製剤投与前後の抗核抗体の変化と抗薬物抗体との関連性の検討
神鋼記念病院膠原病リウマチ科の臨床研究に協力してくださった患者さまへのお願い
過去に当院膠原病リウマチ科の臨床研究への協力してくださった方へお願いです。
当院の臨床研究にご協力いただきましたことを改めましてお礼申し上げます。
その時の成果などを引き継ぎ、この度新たに下記の臨床研究を実施しております。
過去の臨床研究(下記備考欄に記載)への協力に際し、提供して頂きました血液や医療情報の一部を下記の研究に使用致したく存じます。下記の研究対象者に該当する方で、もしも今回の研究への利用を希望されない場合やお問い合わせは、下記の連絡先、または主治医までお申し出下さい。
研究課題名(倫理委員会承認番号)
関節リウマチ患者における生物学的製剤投与前後の抗核抗体の変化と抗薬物抗体との関連性の検討
(No. 1743, 2038)
当院の研究責任者(所属)
熊谷 俊一(神鋼記念病院膠原病リウマチセンター長)
他の研究機関および各施設の研究責任者
他の研究機関は、本研究には属さない
本研究の目的
関節リウマチにおいて生物学的製剤による治療後の検査値(抗核抗体などの自己抗体やMMP3などの疾患活動性マーカー)の変化を検討し、製剤投与後の無効、副作用の出現を予測するのに有用なバイオマーカーを探索する。
調査データ該当期間
2010年4月1日~2026年3月31日
研究の方法(使用する試料等)
●対象となる患者さま
生物学的製剤による治療を受けた関節リウマチ患者
●取り扱う情報
・日常診療での検査用採血の残余血液
・患者背景:疾患名と年齢、性別、既往歴、治療薬
・検査項目:抗核抗体などの自己抗体や、サイトカインなどの疾患活動性マーカー
試料/情報の他の研究機関への提供および提供方法
日常診療の一助として、国内でできない検査を海外の検査会社に依頼する場合がありますが、ID番号や氏名等の個人識別情報は匿名化した上で送付します。
個人情報の取り扱い
利用する情報から氏名や住所等の患者さまを直接特定できる個人情報は削除致します。また、研究成果は学会等で発表を予定していますが、その際も患者さまを特定できる個人情報は利用致しません。
本研究の資金源(利益相反)
本研究に関連し開示すべき利益相反関係にある企業等はありません。
連絡先
電話:078-261-6799
担当者:高橋 宗史、熊谷 俊一
備考
自己免疫疾患病態解析法の多角的検討(2011年3月11日~2013年3月31日)および(2013年4月1日~2015年3月31日)
HAM患者レジストリ「HAMねっと」を活用した病態解明および治療法・予防法の開発に関する研究
「HAM患者レジストリ「HAMねっと」を活用した病態解明および治療法・予防法の開発に関する研究」にご参加いただいた皆様へ
2024年2月20日
当院では、「HAM患者レジストリ「HAMねっと」を活用した病態解明および治療法・予防法の開発に関する研究」に倫理審査委員会の審査を受けて院長の許可を得た上で協力しています。
当該研究は2019年11月から行われており、ご参加いただいた皆様より臨床情報や生体試料、その生体試料から得られる遺伝子データをご提供いただき、研究に活用させていただいております。以下の機関にも生体試料やデータを提供し、共同研究を行っておりますので、提供を希望されない場合は、下記の連絡先にお問合せください。本研究に関する資料の閲覧をご希望の場合も下記の連絡先にお問合せください。
| 機関名 | 研究責任 |
|---|---|
| 難病プラットフォーム | 松田 文彦 |
| 京都大学大学院医学研究科附属ゲノム医学センター | 松田 文彦 |
| 東京大学大学院 新領域創成科学研究科 | 内丸 薫 |
| 熊本大学 ヒトレトロウイルス学共同研究センター | 佐藤 賢文 |
| 金沢大学 医薬保健研究域医学系 | 和田 隆志 |
| 国立研究開発法人医薬基盤・健康・栄養研究所 | 秋丸 裕司 |
| 国立研究開発法人 国立国際医療研究センター | 國土 典宏 |
| 国立感染症研究所 感染症危機管理研究センター/ウイルス第二部 | 斎藤 益満 |
| 熊本大学大学院生命科学研究部 血液・膠原病・感染症内科 | 松岡 雅雄 |
| アメリカ Regeneron社 | Nicole Dossin |
| 田辺三菱製薬株式会社 育薬本部 開発第一部※ | 丸林 冬彦 |
連絡先
聖マリアンナ医科大学 難病治療研究センター
病因・病態解析部門 山野嘉久
〒216-8512 神奈川県川崎市宮前区菅生2-16-1
TEL: 044-977-8111(内線4021)
FAX:044-977-9772
yyamano@marianna-u.ac.jp
進行性の線維化を有する間質性肺炎患者における抗線維化薬の減量・中止に関わる因子の探索及び中止・減量が予後に与える影響の後方視的調査
本件は「オプトアウト」すなわち,同意不要であった既存データを用いた研究において、「自分のデータは使わないでほしい」という、患者さんの拒否の機会を確保するため、研究の公開をホームページ上で行っているものです。 今回の研究に該当されることが予想され、「自分のデータは使わないでほしい」と希望される方はご本人・ご家族より当院に手紙、メール、お電話もしくはファックスなどにてその旨ご連絡ください。
神鋼記念病院呼吸器内科に通院中の間質性肺炎で抗線維化薬を使用した歴のある患者さんへ
実施する臨床研究
抗線維化薬の減量・中止に関わる因子の探索と抗線維化薬の減量・中止が予後に与える影響について調査研究を実施しております。この研究は「観察研究」と呼ばれるもので、 通常の診療で得られた記録をまとめることによって行います。以下の点をご理解いただき、ご協力いただきますようお願い申し上げます。
この研究の意義、目的、および方法
抗線維化薬であるピルフェニドン(ピレスパ錠)、ニンテダニブ(オフェブ錠)は、現在特発性肺線維症(IPF)に対する標準治療となっており、また特発性肺線維症以外の進行性の線維化を有する間質性肺炎に対してもニンテダニブが肺機能低下を抑制する事が2019年に示され、同疾患群へニンテダニブが保険承認されて以降、その処方数が増加してきています。抗線維化薬が間質性肺炎患者の生命予後を改善する可能性を示唆する大規模データも発表されており、今後も進行性の線維化を伴う間質性肺炎に対する処方量は増加していくものと考えられますが、抗線維化薬による副作用や、経済的な理由で処方を継続できない症例もみられます。間質性肺炎に対する抗線維化薬の減量・中止にはどういった因子が関わるかを探り、抗線維化薬の減量・中止が予後にどういった影響を与えたかを知ることで、患者さんにとってより適切な薬剤の管理を行えるよう配慮する事を目的とします。
この研究による医学上の貢献と予測
日常臨床で得られる情報を通して、どういった方にどういった投与量で薬剤を開始し、どの程度の期間継続するべきか、患者さんにとって最適な抗線維化薬の投与方法を検討します。
この研究による患者さんの不利益および危険性
患者さんの診療情報を分析する研究であり、プライバシーも厳重に保護されますので、患者さんに不利益や危険性はありません。
費用や追加の検査
通常の保険診療による画像診断情報と臨床情報の収集と分析ですので、患者さんに余分な費用を負担してもらうことはありません。また、検査方法の変更や追加検査もありません。
個人情報の保護
この研究で得た情報は厳重に管理され、学術目的のみで利用されます。 研究結果は主として統計として処理・解析され発表されるため、個人を特定できることはありません。研究結果の発表に際して、一部の患者さんの臨床情報が参考所見として呈示される可能性がありますが、匿名化されていますので、個人を特定できることはありません。 本研究参加者以外の第三者に流出することもありません。以上のように、患者さんのプライバシーは厳重に保護されますのでご安心ください。
ご協力の拒否について
この研究にご自分のデータが使用されることを拒否される場合は、担当医もしくは下記の問い合わせ先に連絡下さい。 たとえ、協力を拒否されても、今後の診療の不利益になることはありません。しかし、拒否のお申し出のあった時点で、 既に研究結果が論文などで公表されていた場合には、 研究結果を破棄できないことがあります。 この場合でも個人が特定されることはありませんので個人情報は保護されます。
研究責任者
神鋼記念病院 呼吸器内科 門田 和也
当院における連絡先
神鋼記念病院 呼吸器内科 門田 和也
〒651-0072 神戸市中央区脇浜町1丁目4-47
TEL:078-261-6711 ・ FAX:078-261-6931
全国放射線治療症例に基づく放射線治療の実態調査および質評価
この研究の詳細についてお知りになりたい方は、下欄の問い合わせ担当者まで直接お問い合わせください。
なお、この研究の研究対象者に該当すると思われる方の中で、ご自身の試料(例:血液など)や診療情報(例:カルテの情報など)をこの研究に使ってほしくないと思われた場合にも、下欄の問い合わせ担当者までその旨をご連絡下さい。
試料・情報の利用目的及び利用方法
研究の名称
全国放射線治療症例に基づく放射線治療の実態調査および質評価
研究の対象
2013年1月以降に全国の放射線治療施設で、放射線治療施設で放射線治療を受けられた方
研究の目的
全国の放射線治療施設(粒子線治療、ホウ素中性子捕獲療法を含む)で治療を受けた症例の放射線治療に関する情報を収集・集計・分析し、その結果を医療機関に還元することで治療成績や効果の改善をはかり、医療の質の向上に役立てることを目的とします。
研究の期間
研究機関の長による実施許可日から2028年3月まで
他の機関に提供する場合には、その方法
この研究では外部へ試料・情報をWeb登録システム(DIP社)にて登録し、日本放射線腫瘍学会が保管します。特定の個人を照合するための情報は、治療を行った施設のみが保管・管理します。
利用し、又は提供する試料・情報の項目
研究に使用する試料・情報
情報:病歴、治療歴、副作用等の発生状況、カルテ番号 等
放射線治療、化学療法、外科手術などの治療情報、治療結果、生存・死亡情報、再発情報、副作用情報など
利用する者の範囲
機関名および責任者名
浜松医科大学放射線腫瘍学講座 中村和正
(日本放射線腫瘍学会 データベース委員会)
国立研究開発法人量子科学技術研究開発機構
量子生命・医学部門 QST病院 大場久照
国立大学法人大阪大学大学院医学系研究科
生体物理工学講座 沼崎穂高
既存試料・情報の提供のみ行う機関
全国放射線治療施設 約800機関
https://www.rtmapsyu.com/
https://www.jastro.or.jp/medicalpersonnel/data_center/
試料・情報の管理について責任を有する者の氏名又は名称
浜松医科大学放射線腫瘍学講座 中村和正
試料・情報の利用又は他の研究機関への提供の停止(受付方法含む)
あなたの試料または情報を研究に使用することや、他の研究機関に提供することを望まない場合には、問い合わせ先まで連絡をいただければ、いつでも使用や提供を停止することができます。連絡方法は、以下≪問い合わせ先≫をご確認ください。
資料の入手または閲覧
この臨床研究の計画や方法については、あなたのご希望に応じて資料の要求または閲覧ができます。あなたがご自分の研究結果を知りたいと希望される場合は、特定の個人を識別および照合できない情報を使用するため、個人が特定できず、残念ながら対応できません。
情報の開示
あなたご自身が研究の概要や結果などの情報の開示を希望される場合は、他の参加者に不利益が及ばない範囲内で、原則的に結果を開示いたします。しかし、情報の開示を希望されない場合は、開示いたしません。
また、本研究の参加者以外の方が情報の開示を希望する場合は、原則的に結果を開示いたしません。
問い合わせ先
本研究全体についてのお問い合わせ先
〒431-3192
浜松市東区半田山一丁目20番1号
浜松医科大学
部署名: 放射線腫瘍学講座
担当者: 中村和正
TEL: 053-435-2242
E-mail: nakam@hama-med.ac.jp
ご自身で受けた放射線治療に関するお問い合わせ先
〒651-0072
神戸市中央区脇浜町1-4-47
神鋼記念病院 放射線治療科
部署名: 放射線治療科
担当者: 藤代 早月
TEL: 078-261-6711 (平日9:00~17:00)
E-mail: sfuji-6048@shinkohp.or.jp
アベマシクリブ(ベージニオ®)投与患者における有害事象発現のリスク因子に関する研究
当院では、以下の臨床研究を実施しております。この研究は、日常診療で得られた以下の診療情報を研究データとしてまとめるものです。研究のために、新たな検査などは行いません。この案内をお読みになり、ご自身またはご家族がこの研究の対象者にあたると思われる方で、ご質問がある場合、またはこの研究に診療情報を使ってほしくないとのご意思がある場合は、遠慮なく下記の担当者までご連絡ください。
ただし、すでに解析を終了している場合には、研究データから情報を削除できない場合がありますので、ご了承ください。
対象となる方
研究参加施設において、アベマシクリブ(ベージニオ®)が投与された方
研究代表者
市立吹田市民病院 薬剤部 児玉暁人
当院の研究代表者
神鋼記念病院 診療技術部薬剤室 堀端 真次
研究の目的
アベマシクリブ(ベージニオ®)投与後の副作用等により減量及び中止となるリスク因子を探索するとともに予後の危険因子を明らかにすることを目的とします。
利用する診療情報
アベマシクリブ(ベージニオ®)開始時および減量開始時の年齢、性別、身長、体重、併存疾患(糖尿病、免疫疾患など)、ステージ分類、化学療法施行歴、併用薬、血算(白血球数、ヘモグロビン、好中球数、リンパ球数、血小板数)、生化学(Alb、BUN、Cre、Na、K、AST、ALT、CRP、総ビリルビン、総コレステロールなど)、薬剤師外来の有無、予後情報などを診療録から集積し解析します。
外部機関と研究データの共有
上記の診療情報を、次の研究機関と共有して、共同で研究を進めます。
・共同研究機関及び研究責任者
- 1.市立吹田市民病院 薬剤部主幹 児玉暁人
- 2.明石市立市民病院 医療技術部薬剤課 藏本 裕信
研究期間
研究許可日より2028年3月31日まで(予定)
個人情報の取り扱い
お名前、住所などの個人を特定する情報につきましては厳重に管理を行い、学会や学術雑誌等で公表する際には、個人が特定できないような形で使用いたします。
この研究で得られた情報を将来、他の研究機関に提供し二次利用する場合や、研究計画書を変更する場合があります。その場合は、研究倫理審査委員会での審議を経て、研究統括管理責任者の許可を受けて実施されます。その際、文書を公開する場合は、神鋼記念病院 公式サイト(https://shinkohp.jp)の「患者・ご家族の皆様へ 研究情報の公開について」のページに掲載いたします。
問合せ先
神鋼記念病院 診療技術部薬剤室 堀端 真次
電話 078-261-6711(代表)
造影マンモグラフィの乳癌画像診断への適用に関する研究
造影マンモグラフィの乳癌画像診断への適用に関する研究に御参加いただいた方へ
神鋼記念病院 乳腺科
2018年1月より当院乳腺科で継続して参りました臨床研究『造影マンモグラフィの乳癌画像診断への適用に関する研究』は、これまでに289名の方に研究参加のご同意を頂き、 277名の方に検査を実施させて頂きました。皆様には本臨床研究にご理解とご協力を頂き、厚く感謝申し上げます。
昨今、世界的にみると造影マンモグラフィ検査は急速に普及してきました。乳房造影MRI検査に匹敵する乳がん診断能が示されるなど、新しい乳房画像診断法として注目されています。ご参加頂いた本研究においても、乳房造影MRIと比較する事でより正確な腫瘍切除が可能であった手術が多々ありました。また、造影マンモグラフィを行ったことで検出可能となった腫瘍もありました。日本国内では普及している乳房造影MRI検査も、MRI造影剤アレルギーや体内金属、閉所恐怖症などの理由から実施できない患者さんがおられます。そのような方では、造影マンモグラフィが精密検査として威力を発揮することが期待できます。また、乳房造影MRI検査よりも検査時間が短く、費用も安価となることが想定されています。
本研究においては、既に、2018年1月~2019年12月に検査を実施させて頂いた107名の方のうち、術前抗がん剤治療が実施されなかった69名の方について、造影マンモグラフィの診断能の解析結果を2022年7月に公表させて頂いており*1、乳房造影MRI検査と同等の診断能を有していたこと、特に閉経後の乳がん患者さんにおいて有効性が高かったことを報告しました。術前抗がん剤治療を実施頂いた方や2020年以降に研究参加頂いた方の解析結果についても、今後研究成果をまとめる予定です。
*1:Breast Cancer 2022;29(4):677-687. doi: 10.1007/s12282-022-01345-1.
さて、本研究は、目標症例数:300名、研究期間:西暦2025年3月31日までを予定しておりましたが*2、この度2023年4月20日をもちまして終了となりました。改めて、皆様方に厚く御礼申し上げます。終了となりました理由は、本研究の造影マンモグラフィ検査に使用した(1)マンモグラフィ装置(富士フイルム社製 FDR MS-3500)と同装置に搭載されていた(2)エネルギーサブトラクション機能のうち、(2)に対する自主回収の手続きが行われたためです。
*2:2020年3月に認定審査委員会に目標症例数追加・研究期間延長の変更申請し承認。
自主回収の対象となったエネルギーサブトラクション機能は、点滴された造影剤が乳房内に分布する様子を強調するために用いる画像作成機能です。造影マンモグラフィ検査においてエネルギーサブトラクション機能は不可欠であり、乳がんのように血流が豊富な病気の部分を検出することを可能にします。2017年9月に国の薬事認証を取得し、2018年1月より本研究が開始されました。しかしながら、2023年3月に厚生労働省より、日本国内で規定するマンモグラフィ装置の規格(JIS Z 4751-2-451)の適応外項目に乳房造影検査(造影マンモグラフィ検査)が含まれるという指摘がありました。この指摘をうけ、造影マンモグラフィ検査を想定してマンモグラフィ装置(富士フイルム社製 FDR MS-3500)に搭載されているエネルギーサブトラクション機能は、2023年4月末、富士フイルム(株)により自主回収が行われました。
今回の自主回収により、国内において造影マンモグラフィ検査を行うことが当面出来なくなりました。一方、欧州や米国をはじめとする諸外国では、同じマンモグラフィ装置に対し、エネルギーサブトラクション機能の搭載と使用は認証されており、日常の医療現場で使用されています(2017年3月 欧州にて認可、2022年5月 米国FDAにて認可)。また、本機能の全出荷台数(日本9台、海外206台)において、これまでに本機能そのものの品質不良や安全性の問題がないことを合わせてお知らせ申し上げます。当院における研究期間中においても、造影マンモグラフィ検査を実施頂いた277名のうち、1名の方に造影剤の副作用と考えられる軽度の蕁麻疹がありましたが、マンモグラフィ撮影に伴う健康被害はありませんでした。
以上のとおり、本研究で使用しました“エネルギーサブトラクション機能”は一旦自主回収の手続きが行われ研究は終了いたしますが、皆様にご協力頂いた研究データは大変貴重なものであり、本研究成果をまとめ発信し、今後の乳がん診療の精度向上や効率化に活用することが重要であると考えています。そして、海外と同様に国内でも認証され、必要な患者さんに造影マンモグラフィ検査が提供できることを目指してまいります。
自主回収の件につきましては、ご心配やご不安を感じられる方もおられるかと存じます。本研究内容及びこの度のご報告に関しまして、更に詳しいご説明をご要望の場合は、別途機会を設け対面にてご説明申し上げます。もしご希望の場合は、お手数ではございますが下記連絡先までお問い合わせを頂けますようよろしくお願い申し上げます。
問い合わせ先
社会医療法人神鋼記念会 神鋼記念病院 乳腺科
〒651-0072 神戸市中央区脇浜町1-4-47
TEL: 078-261-6711
研究責任医師:乳腺科 医長 結縁 幸子
EGFR遺伝子L858R変異陽性非小細胞肺癌に対するラムシルマブ+エルロチニブ療法の有効性と安全性に関する研究のお知らせ
神鋼記念病院では以下の研究を行います。
本研究は、倫理委員会の審査を受け承認された後に、関連の研究倫理指針に従って実施されるものです。
研究期間: 2023年2月21日 ~ 2026年12月31日
研究課題
EGFR遺伝子L858R変異陽性進行再発非扁平上皮非小細胞肺癌に対するRamucirumab + Erlotinibの有効性及び安全性を評価する多機関共同・後方視的観察研究(REAL-SPEED)
研究目的
実臨床での使用実績に基づいてEGFR遺伝子L858R変異陽性非小細胞肺癌に対するRamucirumab+ Erlotinib療法を、有効性および安全性の面で優れているか後ろ向きに調査することで、より適切な使用法を検証することを目的とします。
研究意義
日本人におけるEGFR遺伝子L858R変異陽性非小細胞肺癌での有望な治療オプションの幅が広がる可能性を追求します。
対象・研究方法
2020年11月1日から2023年6月30日までに一次治療としてラムシルマブ+エルロチニブ療法が開始された患者様。肺癌に対する治療を評価するため、上記の患者様から重複癌(例:胃癌と肺癌を同時に患っている)を除いた方が対象となります。主要評価項目は治療成功期間となります。
研究機関名
当院を含む55機関と代表機関である帝京大学医学部内科学講座
個人情報の取り扱い
本研究に携わる関係者は研究対象者の個人情報を厳格に保護します。対象者より情報の使用拒否の申し出があった場合はその情報は用いず破棄します。研究用ID(研究対象者識別コード)とすることで個人が特定されないように情報を加工し、抽出したデータのみを取り扱うことで個人の特定ができないようにします。お亡くなりになった方の情報についても同様に取り扱い対象者が特定できないよう十分に配慮します。対象となる患者様で、ご自身の検査結果などの研究への使用をご承諾いただけない場合や、研究についてより詳しい内容をお知りになりたい場合は、下記の問い合わせ先までご連絡下さい。ご協力よろしくお願い申し上げます。
問い合わせ先
当院における研究責任者:氏名 大塚 浩二郎 職名 呼吸器内科部長
所属:神鋼記念病院
住所:神戸市中央区脇浜町1-4-47 TEL:078-261-6711
一般病院からがんゲノム医療連携病院へ依頼する包括的がんプロファイル検査の現状と問題点
神鋼記念病院の患者さんへ
本件は「オプトアウト」すなわち、既存データを用いた研究において、「自分のデータは使わないでほしい」という患者さんの拒否の機会を確保するため研究の公開をホームページ上で行っているものです。今回の研究に該当されることが予想され、「自分のデータは使わないでほしい」と希望される方は、ご本人・ご家族より当院にその旨ご連絡ください。
研究課題名
一般病院からがんゲノム医療連携病院へ依頼する包括的がんプロファイル検査の現状と問題点
1.研究の目的・意義
一般病院で治療中の癌患者をゲノム医療に繋げるにはがんゲノム医療連携病院(連携病院)へ紹介する必要がある。本研究の目的は当院から連携病院へ包括的がんプロファイル検査を依頼した症例を解析し問題点を明らかにすることです。
2.情報の取得期間
2021年4月〜2023年3月までに当院から連携病院へ包括的がんプロファイル検査を依頼した方が対象となります。
3.診療情報の項目
年齢、性別、治療内容などに関してカルテより得られた情報を利用します。
4.解析結果は学会発表、学術論文として公表いたします。
5.個人情報の保護
この研究で得た情報は厳重に管理され、学術目的のみで利用されます。従って、学会発表や論文から個人が特定される恐れはありません。本研究参加者以外の第三者に個人情報が流出することもありません。各患者さんのプライバシーは厳重に保護されますのでご安心ください。
6.利益相反
私共の研究に関して、個人や会社との利益相反はありません。
7.研究への参加を拒否される場合は、当院の下記担当者までご連絡ください。
当院における連絡先: 神鋼記念病院 がんゲノム外来 藤本 康二
〒651-0072 神戸市中央区脇浜町1丁目4-47
Tel: 078-261-6711、FAX: 078-261-6726
過敏性肺炎の全国疫学調査
2021年1月1日~2021年12月31日に過敏性肺炎疾患で受診した患者さんへ
~研究協力のお願い~
(1)研究の概要について
承認番号: 第 M2022-045 番
研究課題名:過敏性肺炎の全国疫学調査
研究期間: 医学部倫理審査委員会承認後から西暦2027年3月31日
研究責任者:東京医科歯科大学 統合呼吸器病学分野 教授 宮崎 泰成
本研究は東京医科歯科大学医学部倫理審査委員会の承認及び機関の長の許可を得て実施されています。
<研究の概略>
種々の抗原により発症するアレルギー性の間質性肺炎を過敏性肺炎と言います。線維性過敏性肺炎は進行すると労作時息切れを自覚し長期の療養が必要となり、線維化の進んだ過敏性肺炎の平均生存期間は3年弱と予後不良です。また、本症は小児期にも発症し呼吸不全を来たし肺移植を受けている患者さんもいることが知られており、小児から成人に至る詳細な臨床像は明らかにされていません。
この過敏性肺炎は現在まで十分な疫学調査が行われておりません。患者数は1〜2万人いると考えられていますが、これまで患者数を推定するための全国疫学調査は行われておりません。また、今まで確立した診断法はありませんでしたが、日本呼吸器学会より「過敏性肺炎診療指針2022」が2022年4月に発刊され、診断が標準化されました。本研究では、「過敏性肺炎診療指針2022」に基づいて疫学調査を行うことで、過敏性肺炎の正確な有病率および罹患率、疾患特性を明らかにしたいと考えております。
(2)研究の意義・目的について
1991年、1999年、2013年に厚生労働省政策班主導で疫学研究が行われております。しかし、これらは主要な医療施設に限定された調査であったため正確な有病率や罹患率が出せませんでした。そしてその後ほぼ10年間疫学調査は行われておりません。本研究は、「過敏性肺炎診療指針2022」に基づいて疫学調査を行うことで、①2022年4月に発刊された過敏性肺炎診療指針の検証、改定に向けた調査、客観的な診断基準・重症度分類の策定、②有病率・罹患者数の推定、③小児から成人への移行期医療体制の構築、を行うことを目的とします。
(3)研究の方法について
事前に一次調査の際に各ご施設より回答いただきましたが、二次調査へ協力する旨の返答があった施設において、患者個人調査票への回答を依頼します。調査対象は、東京医科歯科大学および二次調査への協力施設において、2021年1月1日~2021年12月31日に過敏性肺炎疾患で受診した患者さんとします。性別、年齢に制限を設けません。予定症例数は1000例としますが、制限を設けるものではありません。
本来であれば患者さん個別に御説明した上で御同意を頂くところですが、この掲示によって替えさせて頂きます。
患者さんの診療録から研究のために以下の情報を取得します。①生年月日、②性別、③年齢、④人種・地域、⑤喫煙に関して、⑥曝露抗原情報(住居環境、周辺環境、職業歴、趣味など)、⑦家族歴、⑧既往歴、⑨発症様式(線維性、非線維性、急性、亜急性、慢性、無症状)、⑩自覚症状(発熱、咳、痰、労作時呼吸困難、mMRCスケール)、⑪身体所見(身長、体重、酸素飽和度、呼吸音、ばち指、膠原病関連の身体所見)、⑫血液検査所見(白血球数、CRP、ALB、LDH、KL-6、SP-D、膠原病関連自己抗体、鳥IgG、トリコスポロンアサヒ抗体など)、⑬動脈血液ガス分析、⑭呼吸機能検査(VC, %VC, FVC, %FVC, DLCO, %DLCO, ΔVC, ΔFVC)⑮6分間歩行試験、⑯気管支肺胞洗浄、⑰抗原回避試験、⑱抗原誘発試験、⑲画像所見:胸部CT所見、⑳病理検査所見、㉑治療経過、㉒急性増悪の有無、㉓病歴、㉔診断根拠。検査データにおいては診断時のものに加え12か月後、24か月後、36か月後、48か月後、60か月後のものも収集します。データは東京医科歯科大学のeACReSSという情報データシステムを用いた患者調査票を使用します。これらの情報は日常診療で行っている検査結果などから取得するため、本研究のために追加で検査していただくことはありません。その他研究目的で採血以外に追加で行っていただく検査はなく、薬の投与などもありません。胸部CT画像および病理組織標本は東京医科歯科大学呼吸器内科に送付し集約されます。
(4)試料・情報等の保管・廃棄と、他の研究への利用について
抽出した情報は、個人が特定できないよう、番号に置き換え匿名化したうえで研究者が責任をもって10年間、責任者の研究室に保管、管理します。既存試料・情報のみを提供する機関においても同様に、研究対象者をカルテ上でピックアップした後、個人が特定できないよう番号に置き換え匿名化したうえでeACReSSに情報を集約します。
保存期間を超えた情報は匿名化されたまま廃棄します。データは学会発表と論文作成のみに使用し、前述以外の使用目的には一切使用しません。本研究で得られた情報を別の研究に二次利用する際は、新たな研究計画を立案時点で医学部倫理審査委員会に諮り、承認を得られた後に、東京医科歯科大学生命倫理研究センターのHPおよび二次調査へ協力いただいた施設でポスター掲示を行います。
(5)予測される結果(利益・不利益)について
すでに診療録上に登録されている情報を使用するため健康を害する可能性はありません。御参加頂いた個人の方に、診療の上で利益や不利益となることはありません。
なお、本研究への参加を断っても、病院での診療等に不利益はありません。
(6)研究協力の任意性と撤回の自由について
この研究に参加するかどうかは、あなたの自由意思によって決めていただくことになります。このポスターをご覧になって自分のデータを研究に使用してほしくない場合には、下記連絡先に申し出て下さい。たとえ同意いただけない場合であっても、不利益を受けることは決してありません。
また、本研究に診療情報を使用してほしくないというご連絡をいただいた場合には、それまでに保存されたデータは廃棄されます。但し、保存されたデータを使用し、すでに研究結果が論文などで公表されている場合には、その結果を廃棄できない場合がありますのでご了承下さい。
(7)個人情報の保護・取り扱いについて
データは個人が特定できないよう、番号に置き換え匿名化した状態で解析します。各番号に対応した個人名を記した対応表は研究責任者のパソコンのみでの閲覧に限定して厳重に管理します。各研究協力機関との診療録上の情報の授受に際しても同様に、個人が特定できないよう、番号に置き換え匿名化した状態で行います。各番号に対応した個人名を記した対応表は研究責任者のパソコンのみでの閲覧に限定して厳重に管理します。
(8)研究に関する情報公開について
皆様の協力によって得られた貴重なデータは、個人情報を消去した形で国内外の医学系学会や学術論文で公に発表させて頂きます。
(9)研究によって得られた結果のお知らせ
この研究で得られた結果を患者さんにお知らせする予定はありません。
(10)経済的な負担および謝礼について
この研究は診療録上にすでに登録されている情報のみを用いるため、研究に参加することによる新たな費用負担はありません。また謝礼もありません。
(11)研究資金および利益相反について
利益相反とは、研究者が企業など、自分の所属する機関以外から研究資金等を提供してもらうことによって、研究結果が特定の企業にとって都合のよいものになっているのではないか・研究結果の公表が公正に行われないのではないかなどの疑問が第三者から見て生じかねない状態のことを指します。研究の実施にあたっては、東京医科歯科大学利益相反マネジメント委員会に対して研究者の利益相反状況に関する申告を行い、同委員会による確認を受けています。
本研究は、国立研究開発法人日本医療研究開発機構(AMED)からの資金および当研究室の運営費で実施されます。
(12)研究に係るご相談・問い合わせ等の連絡先
研究者連絡先:神鋼記念病院 呼吸器内科 医長 門田 和也
所在地:兵庫県神戸市中央区脇浜町1-4-47
電話番号:078-261-6711(代表) (対応可能時間帯:平日9:00~17:00)
苦情窓口:同上(対応可能時間帯:平日9:00~17:00)
※他の研究参加者の個人情報や研究の独創性の確保に支障が生じない範囲内で、研究計画書や研究の方法に関する資料を閲覧することができます。ご希望の際は、上記の研究者連絡先までお問い合わせください。
当院におけるロボット支援腹腔鏡下前立腺全摘術における術後の腸閉塞およびイレウスの発生率と危険因子についての検討
神鋼記念病院泌尿器科の患者さんへ
1.研究の目的・意義
ロボット支援腹腔鏡下前立腺全摘術(以下RARP)における術後合併症として腸閉塞およびイレウスが挙げられます。保存的加療で改善するもののみではなく、外科的加療の必要なものもあり、重大な合併症となり得ます。そこでRARP術後における腸閉塞およびイレウスの頻度と危険因子を検討することを目的とします。
2.情報の取得期間
2015年11月1日から2023年3月31日の間に当院でRARPを受けられた患者様を対象とします。
3.診療情報の項目
RARPを受けられた患者様の臨床情報(年齢、身体所見、検査結果、手術時の情報、入院中の情報、画像所見、経過観察期間、転帰)について、診療録をもとに匿名化した状態で、解析に用います。
4.解析結果は学会発表、論文として公表いたします。
5.個人情報の保護
この研究で得た情報は厳重に管理され、学術目的のみで利用されます。従って、学会発表や論文から個人が特定される恐れはありません。本研究参加者以外の第三者に個人情報が流出することもありません。各患者さんのプライバシーは厳重に保護されますのでご安心ください。
6.利益相反
私共の研究に関して、個人や会社との利益相反はありません。
7.研究への参加を拒否される場合は、当院の下記担当者までご連絡ください。
当院における連絡先: 神鋼記念病院 泌尿器科
〒651-0072 神戸市中央区脇浜町1丁目4-47 Tel: 078-261-6711, FAX: 078-261-6726
泌尿器科: 坂田 宏行
SARS―CoV2ワクチン接種後に生じたリウマチ性疾患についての全国調査
神鋼記念病院膠原病リウマチ科の患者さんへ
2023年2月 神鋼記念病院膠原病リウマチ科
この度、日本リウマチ学会では、本邦における新型コロナウイルス(SARS-CoV2)に対するワクチン接種後に生じたリウマチ性疾患の実態を明らかにするため、全国調査を行うこととなりました。九州大学別府病院内科を中心に行われている同観察研究に当院も協力しております。
1.観察研究について
九州大学病院では、最適な治療を患者さんに提供するために、病気の特性を研究し、診断法、治療法の改善に努めています。患者さんの生活習慣や検査結果、疾病への治療の効果などの情報を集め、これを詳しく調べて医療の改善につながる新たな知見を発見する研究を「観察研究」といいます。その一つとして、九州大学病院別府病院内科では、現在 SARS-CoV2 ワクチン接種後に生じたリ ウマチ性疾患の患者さんを対象として、従来のリウマチ性疾患と異なるものかどうかに関する「観察研究」を行っています。今回の研究の実施にあたっては、九州大学医系地区部局観察研究倫理審査委員会の審査を経て、研究機関の長より許可を受けています。この研究が許可されている期間は、2023年12月31日までです。
2.研究の目的・意義
新型コロナウイルス感染症(COVID-19)の流行に伴い、初めてメッセンジャーRNA ワクチンという新しい種類のワクチンが実用化されました。従来のワクチン(インフルエンザワクチンなど)を接種した後にリウマチ性疾患、すなわち免疫の異常によっておこる病気を発症する人が極稀にいることが報告されています。新しいワクチンについては未知数ですが、欧米からはメッセンジャーRNAワクチンを接種した後にリウマチ性疾患を発症したという例が少数ながら報告されています。日本で同様のことがどのくらいの方に起こっているのか、通常のリウマチ性疾患と症状や経過が異なるかについては全くわかっていない状況です。そこで今回、九州大学病院別府病院内科では全国の日本リウマチ学会教育施設に対し、新型コロナウイルス(SARS-CoV2)に対するワクチン(以下コロナワクチン)接種後に発症したリウマチ性疾患の患者様の実態を調査するべく、本研究を計画しました
3.研究の対象者について
2021年1月1日から 2022年6月30日の期間に当施設を受診された方のうち、コロナワクチン1回目または2回目接種後28日以内にリウマチ性疾患を発症したと診断された方が対象です。研究の対象者となることを希望されない方又は研究対象者のご家族等の代理人の方は、事務局までご 連絡ください。
4.研究の方法について
この研究を行う際は、カルテより以下の情報を取得します。取得した情報を分析し、コロナワクチンのリウマチ性疾患の発症に対する影響を明らかにします。
〔取得する情報〕
年齢、性別、身長、体重、リウマチ性疾患の既往歴、ワクチンの種類、リウマチ性疾患の発症時期、リウマチ性疾患の診断名、国際的診断基準を満たしていたかどうか、重症度はどの程度か、治療内容(ステロイド、免疫抑制剤の使用の有無や量)、3 回目コロナワクチン接種時の状況(リウマチ性疾患が増悪したか、接種時に治療継続していたか)、その他主治医が経過において重要と認めた内容(既往歴、家族歴など)
それらの各医療機関での情報を九州大学病院別府病院内科で収集、解析します。
5.個人情報の取り扱いについて
研究対象者のカルテの情報をこの研究に使用する際には、容易に研究対象者が特定できる情報を削除して取り扱います。この研究の成果を発表したり、それを元に特許等の申請をしたりする場合にも、研究対象者が特定できる情報を使用することはありません。この研究によって取得した情報は、九州大学病院別府病院内科・教授・堀内 孝彦の責任の下、厳重な管理を行います。
6.資料や情報の保管等について
〔情報について〕
この研究において得られた研究対象者のカルテの情報等は原則としてこの研究のために使用し、研究終了後は、九州大学病院別府病院内科において同分野教授・堀内 孝彦の責任の下、10年間保存した後、研究用の番号等を消去し、廃棄します。
また、この研究で得られた研究対象者の情報は、将来計画・実施される別の医学研究にとっても大変 貴重なものとなる可能性があります。そこで、前述の期間を超えて保管し、将来新たに計画・実施される医学研究にも使用させていただきたいと考えています。その研究を行う場合には、改めてその研究計画を倫理審査委員会において審査し、承認された後に行います。
7.利益相反について
九州大学では、よりよい医療を社会に提供するために積極的に臨床研究を推進しています。そのため の資金は公的資金以外に、企業や財団からの寄付や契約でまかなわれることもあります。医学研究の発展のために企業等との連携は必要不可欠なものとなっており、国や大学も健全な産学連携を推奨しています。一方で、産学連携を進めた場合、患者さんの利益と研究者や企業等の利益が相反(利益相反)してい るのではないかという疑問が生じる事があります。そのような問題に対して九州大学では「九州大学利益相反マネジメント要項」及び「医系地区部局における臨床研究に係る利益相反マネジメント要項」を定めています。本研究はこれらの要項に基づいて実施されます。 本研究に関する必要な経費は部局等運営経費であり、研究遂行にあたって特別な利益相反状態にはありません。
利益相反についてもっと詳しくお知りになりたい方は、下記の窓口へお問い合わせください。
利益相反マネジメント委員会
(窓口:九州大学病院 ARO 次世代医療センター 電話:092-642-5082)
8.研究に関する情報の開示について
この研究に参加してくださった方々の個人情報の保護や、この研究の独創性の確保に支障がない範囲で、この研究の研究計画書や研究の方法に関する資料をご覧いただくことができます。資料の閲覧を希望される方は、ご連絡ください。
9.研究の実施体制について
この研究は以下の体制で実施します。
| 研究実施場所 | 九州大学病院別府病院内科 | |
| 研究責任者 | 九州大学病院別府病院内科・教授・堀内 孝彦 | |
| 研究分担者 | 九州大学病院別府病院内科・医員・日浦 惇貴 | |
| 共同研究機関等 | 神鋼記念病院 /科長 籏智さおり | 役割 |
| 全国の日本リウマチ学会教育施設 | 情報の収集 |
10.相談窓口について
この研究に関してご質問や相談等ある場合は、下記担当者までご連絡ください。
事務局 担当者:九州大学病院別府病院内科・医員・日浦 惇貴
(相談窓口) 連絡先:
〔TEL〕0977-27-1640
〔FAX〕0977-27-1641
メールアドレス:hiura.junki.002@m.kyushu-u.ac.jp
神鋼記念病院相談窓口
担当者:膠原病リウマチ科・科長・籏智さおり
連絡先:
〔TEL〕078-261-6711(代表) 平日 9:30〜17:00
〔FAX〕078-261-6726
椎骨動脈スタンプ症候群に対する血管内治療
当院にで脳梗塞で入院された患者さん・ご家族様へ
研究へのご協力のお願い
2023年1月6日
当院では、以下の臨床研究を実施しております。この研究は、日常診療で得られた以下の診療情報を研究データとしてまとめるものです。研究のために、新たな検査などは行いません。この案内をお読みになり、ご自身またはご家族がこの研究の対象者にあたると思われる方で、ご質問がある場合、またはこの研究に診療情報を使ってほしくないとのご意思がある場合は、遠慮なく下記の担当者までご連絡ください。ただし、すでに解析を終了している場合には、研究データから情報を削除できない場合がありますので、ご了承ください。
対象となる方
2021年4月1日から2022年10月31日に、当院に脳梗塞の診断で入院された患者さん
その内、椎骨動脈スタンプ症候群と診断された3名に対し、以下の解析を行っています。
研究課題名
椎骨動脈スタンプ症候群に対する血管内治療
研究責任者
神鋼記念病院 崎須賀涼
研究の目的
脳梗塞の原因の一つとして、椎骨動脈起始部の急性閉塞により血栓塞栓症を繰り返す病態があり、椎骨動脈スタンプ症候群と呼ばれていますが、未だどのように治療を行うべきかという標準治療法が確立されていません。この研究は脳梗塞で治療を行った患者の診療録を後方視的に解析し、椎骨動脈スタンプ症候群の疫学、診断、治療について考察することを目的としています。
利用する診療情報
- 年齢、性別
- 内科的背景、臨床症状
- 治療に用いた薬剤
- 脳梗塞/閉塞血管の部位
- 発症時期
- 血管内治療の方法
- 治療後の転帰
研究期間
研究許可日より2024年3月31日まで(予定)
個人情報の取り扱い
お名前、住所などの個人を特定する情報につきましては厳重に管理を行い、学会や学術雑誌等で公表する際には、個人が特定できないような形で使用いたします。
問合せ先
神鋼記念病院 脳神経外科 担当医師 崎須賀 涼
電話 078-261-6711(代表)
特発性間質性肺炎における赤血球容積分布幅と肺高血圧症の関連についての単施設後方視的コホート研究
はじめに
この文書は「特発性間質性肺炎における赤血球容積分布幅と肺高血圧症の関連についての単施設後方視的コホート研究」の研究事業への、御協力をお願いするための説明文です。
1.研究の背景について
肺高血圧症は早期診断が困難な疾患です。間質性肺炎の患者さまにおいて肺高血圧を合併すると予後が短くなるとされており、肺高血圧を事前に予測することは間質性肺炎の患者さまの診療において重要な課題です。
赤血球容積分布幅(RDW)は体を循環している血液中の赤血球の容積にどのぐらいばらつきがあるかを反映するデータです。当院では通常の血液(血球)検査の際に自動的に計測しています。RDWは、赤血球がつくられるのが亢進しているときやうまく作り出せないとき、こわれる赤血球が通常より増えているとき、壊れた赤血球の除去が遅れているときなどに上昇するデータです。お体が低酸素にさらされているとき、鉄の代謝バランスが崩れているとき、心不全、腎不全、慢性炎症性疾患があるとき、などに異常値を示すことがあるとされています。間質性肺炎の一種である特発性肺線維症や、左心不全、肺動脈性肺高血圧症の患者さまにおいては、RDWが上昇していることは予後が短いことと関係しているという報告があります。しかしながら、間質性肺炎の患者さまにおいてRDWが上昇していると、肺高血圧を現時点で起こしていたり、将来起こしやすくなったりするかどうかは、まだはっきりしていません。
2.研究の目的について
この研究事業の主な目的は、間質性肺炎の患者さまのこれまでのカルテを参照し、RDWが肺高血圧症の有無や将来の肺高血圧症発症の予想につながるかどうかを解析して、間質性肺炎の患者さまに肺高血圧に関するより多くの情報を提供できるようにすることです。
間質性肺炎の患者さまにおいてRDWと肺高血圧症の関係は未だ解明されていませんが我々はRDWが高い患者さまでは肺高血圧をすでに発症していたり、将来発症しやすくなる可能性があがったりするのではないかと考えています。このような研究には、間質性肺炎で通院しておられる多くの方のカルテを参照し、さまざまな患者さまの違いを調べて、RDWと肺高血圧症の関係を解析する必要があります。将来的にRDWと肺高血圧症の関係が明らかになれば、肺高血圧をより早期に見つけて適した治療法を御提案したりできるようになると考えます。
3.研究の方法について
研究にご賛同いただける患者さまについては、カルテ上の年齢、性別、職業、住環境、喫煙歴、身長、体重、既往歴、在宅酸素使用の有無、採血、動脈血液ガス、呼吸機能検査、6分間歩行検査、胸部単純X線、胸部CT、心電図、経胸壁心臓超音波検査、右心カテーテル検査、肺換気血流シンチグラフィー、治療内容、予後を参照し、集積した上で解析します。あなたに必要な通常の診療以上に、追加検査や治療をお願いすることはありません。研究内容の詳細についてお知りになりたい場合は、神鋼記念病院倫理委員会で承認を受けた研究計画書をもとに、その概要を説明させて頂きます。
4.研究期間について
神鋼記念病院院長承認年月日から令和5年9月30日まで。
5.研究機関について
神鋼記念会 呼吸器内科
(神戸市中央区脇浜町1丁目4-47 電話 078-261-6711)
(研究責任者) 神鋼記念会 呼吸器センター 稲尾 崇
(共同研究機関) 当院のみでの研究であり、ありません。
集められた情報は当神鋼記念病院呼吸器内科において厳重に保存・管理されます。情報の取り扱いや利用目的が妥当であることについて,倫理委員会によって審査されています。
6.研究中及び終了後のデータ・試料等の取り扱いについて
あなたのデータ・試料の保存方法についての詳細をお知りになりたければ研究計画書をご覧下さい。本研究が終了した時点で,速やかに試料等は廃棄いたします。しかしながらもしもあなたが同意してくだされば,将来の医学研究のための貴重な資源として,研究終了後も保管させていただきたいと思います。この場合も後述の9.で説明いたします方法により,分析を行う研究者には,どこの誰の試料であるかを分からないようにしたままで,試料が使い切られるまで保管します。
7.予測される研究結果と試料提供者の利益・不利益について
本研究の成果は,現時点ですぐにはあなたに直接利益を与えるものではありませんが,肺高血圧症発症の仕組みの一端を解明し,よりきめ細かい診療と治療を可能にするために貢献するものと期待されます。本研究ではこれまでに当院で診療をうけられた方の診療情報をもとに行うものであり、あらたに研究のために追加の検査や治療を受けていただく必要はありません。
また,後述の9.のような厳重な配慮にもかかわらず,万一個人の情報が外部に漏洩した場合,プライバシーの侵害に始まる,種々の不利益が生じる可能性は否定できません。このような漏洩を行った場合,我々は厳重に処罰されることになっております。神鋼記念病院 呼吸器センターではこうした情報管理について細心の注意を払っており,個人の情報を処理するコンピューターは,他の一切のコンピューターと切り離され,情報は外部記憶装置に保存され,個人情報管理者によって厳重に保管されます。
8.研究協力の任意性と撤回の自由について
言うまでもなく研究への協力をする,しないは完全にあなたの自由意思に任せられており,如何なる意味でも強制されるものではありません。もちろん,同意されなくても、あなたの不利益になるようなことは一切ありません。また,一旦同意した場合でも,あなたが不利益を受けることなく,いつでも同意を取り消すことができ,その場合はあつめられたデータからあなたのデータは削除され,それ以降は研究目的に用いられることはありません。ただし,同意を取り消した時,既に研究結果が論文などで公表されていた場合などには,データの削除ができない場合があります。
9.個人情報の保護について
診療録情報を用いた研究結果は,さまざまな問題を引き起こす可能性があるため,他の人に漏れないように,取り扱いを慎重に行う必要があります。あなたの診療録情報から,分析する前に,住所,氏名,カルテ番号,電話番号などあなた個人を特定できる情報を削除し,代わりに新しく符号を付けます。こうすると,あなたの臨床情報は,分析を実際に行う研究者にとって,誰のものかは全く分からなくなります。これを「匿名化」と呼び,神鋼記念病院呼吸器センターにおいて「個人情報管理者」として指名された者(神鋼記念病院 稲尾 崇)が責任をもって行います。ただしあなたが希望されたり,我々が医学上必要と考えたりして,研究結果についてあなたに説明する場合には,必要な場合に限りこの符合を元の氏名などに戻すことを可能にしてあります。(これを「連結可能」と呼びます。)この操作も上記の「個人情報管理者」の厳重な管理のもとに行います。
10.本研究の結果をお知らせすること(開示)について
本研究は多くの方の協力を得て,間質性肺炎に罹っている方においてRDWが肺高血圧症の有無や発症の予測を可能とするか、多くの患者さまで比較検討するものです。基本的には統計的な比較であり,またなんらかの違いが見出されたとしても,その違いと予後との関係やその後の治療効果を明らかにするためには,まだまだ多くの研究が必要となります。したがってこの研究に参加してくださる個々の方々について,原則として解析結果をお知らせすることはいたしません。また、折角ご協力頂きましても,患者さまのご状態により、最終的に本研究に組み入れられない場合もあり得ます。
ただし,研究の成果によりRDWと肺高血圧発症との関連がほぼ確実になった場合、希望されればその結果をお知らせした上で、その情報に応じた肺高血圧診療の御提案を行うことも可能です。研究の進み具合やその成果,学術的な意義について,あなたが説明を求められる場合には主治医を通して御請求いただければ,研究責任者が分かりやすい形で説明します。
11.研究成果の公表について
あなたの協力によって得られた研究の成果は,学会発表や学術雑誌及びデータベース上(インターネットなど)で公に発表されることがあります。ただしあなた個人を特定できる情報(氏名や住所やカルテ番号)が公表されることは一切ありません。
12.研究から生じる知的財産権の帰属について
将来,本研究全体の成果が新しい発見や特許などに関係する特殊な権利を生み出す可能性がありますが,その場合,その権利は国や研究者などに属し,あなた個人には帰属しません
13.費用負担について
ここで行われる解析研究に必要な費用は,神鋼記念会 神鋼記念病院 呼吸器センターの研究費などから出され、あなたの負担にはなりません。一方、一般診療に要する費用のうち自己負担分についてはあなたが負担しなければなりません。
14.謝礼等について
研究に協力していただけることに対する金銭を含めた報酬は一切なく,交通費などの支給も行いません。
15.研究計画書等の開示について
あなたの希望により,本研究の研究計画書を入手・閲覧できます。
16.カウンセリングの実施について
病気のことや本研究に関して,不安に思うことがあったり,相談したいことがあったりする場合は,専門家の相談を受けることができます。主治医,あるいはこの文書の説明担当者にその旨申し出てください。研究責任者(稲尾 崇)がご説明致します。
17.同意の手順について
この研究事業の内容は、「特発性間質性肺炎における赤血球容積分布幅と肺高血圧症の関連についての単施設後方視的コホート研究同意書」へのご署名あるいは電話での口頭同意をもって同意を得たことといたします。お亡くなりになった患者様や他院に転医され当科での診療が終了している患者様、電話連絡がつかない患者様につきましては、当院倫理委員会の了承の上この文書を当院ホームページ上へ開示し、研究担当医が患者さまの診療録を参照することに詳細に同意をいただいたものとさせていただきます。
あなたがこの説明をよく理解でき、研究事業に協力することには同意できない、とお考えになる場合には、「研究協力の非同意」を研究担当医にお伝えいただくことで、同意の撤回を行うことができます。その場合、あなたの診療録に基づいたデータは研究から除外され、解析にはかけられません。
18.お問い合わせ先について
研究協力への同意を撤回される場合や,研究に関する問い合わせや苦情がおありの時は主治医あるいはこの文書の説明担当者か下記のお問い合わせ先まで御連絡ください。
神鋼記念病院 呼吸器センター 稲尾 崇
電話:078-261-6711(代表)平日9時-17時
令和 4 年 11月 28 日
〒650-0072 神戸市中央区脇浜町1-4-47
神鋼記念病院呼吸器センター
研究責任者:稲尾 崇
「京都造血幹細胞移植グループの造血幹細胞移植データを用いた移植成績の解析」についてのご説明
神鋼記念病院において造血幹細胞移植を受けられた患者さんへ
この文書は、神鋼記念病院において造血幹細胞移植を受けた患者さんの臨床情報について、日本造血細胞移植データセンターから返却の手続きを行い、データ収集及び解析を行うことについての同意をお願いするものです。以下の点をご理解いただき、ご協力いただきますようお願い申し上げます。なお、本研究は「ヘルシンキ宣言」に基づく倫理的原則に則り、「人を対象とする生命科学・医学系研究に関する倫理指針」を遵守して実施しています。また、本研究はすべての参加施設での倫理委員会にて承認を受けております。
1.研究の目的
造血幹細胞移植は難治性造血器腫瘍の根治療法として確立しており、ドナーソースの多様化や高齢者への適応拡大を通じて移植の件数は増大傾向にあります。しかし、未だに移植関連死亡や移植中の感染症管理などの問題が残っており、今後の移植成績の改善のためには予測因子の解析や治療に使用する薬剤等についての継続的な研究が重要です。その様な研究には、患者さんの臨床データの蓄積が必要なため、単一施設における移植の解析には限界があります。
そこで、京都大学医学部附属病院血液内科と関連病院は京都造血幹細胞移植グループを立ち上げ、移植についての臨床的な解析・検討を共同で行っています。京都造血幹細胞移植グループで登録された多数の移植症例を解析することにより、各疾患や移植ソースに対する同種移植に関する移植成績や予後予測因子を明らかにし、今後の移植成績改善のための有用な情報を得ることが目的です。
そして、本研究においては、生存や再発、非再発死亡、移植片の生着。移植片対宿主病などに影響を及ぼす因子を検討します。
2.研究期間
研究期間は1986年1月1日から2025年3月31日までの間に、京都造血幹細胞移植グループ所属施設において、自家・同種造血幹細胞移植を行った症例を対象とする。
- 研究対象者登録期間:研究機関の長の実施許可日から2025年3月31日
- 研究対象者観察機関:登録日から2026年3月31日
- 研究実施期間(総研究期間):2017年4月17日~2027年4月16日
3.研究に用いる情報の種類
年齢、性別、原疾患、治療内容、治療効果、各種検査結果、合併症の有無、移植前後の臨床経過等
診療において実施された検査結果や情報を用いるため、追加の検査はありません。患者さんから得られた検体(血液や細胞)そのものを用いた研究は含まれません。
4.情報の利用方法
日本造血・免疫細胞学会および日本造血細胞移植データセンターが実施する「造血細胞移植および細胞治療の全国調査(TRUMP)」(京都大学の承認番号:R1343)について同意を頂いた患者さんについては、疾患や移植についてのデータが日本造血細胞移植データセンターにおいて収集・データセットに登録されています。このデータセットについては、患者さんの同意がある限り返却してもらうことが可能です。
1986年1月1日から2025年3月31日までの間に、京都造血幹細胞移植グループ所属施設において、自家・同種造血幹細胞移植を行った患者さんのうち、「造血細胞移植および細胞治療の全国調査(TRUMP)」(京都大学の承認番号:R1343)に同意され、かつ、本研究「京都造血幹細胞移植グループの造血幹細胞移植データを用いた移植成績の解析」に同意いただいた場合、日本造血細胞移植データセンターから毎年1回京都大学血液・腫瘍内科データセンターへあなたの全移植データが返却されます。返却された京都造血幹細胞移植グループ全体の移植データを用いて、京都大学血液・腫瘍内科データセンターで新規にデータセットを作成します。
本研究「京都造血幹細胞移植グループの造血幹細胞移植データを用いた移植成績の解析」を行う場合は、各共同研究者が新規に作成されたデータセットを使用します。二次調査は、各共同研究者を通じて病院の電子カルテ情報等を基に追加情報を収集させていただきます。
5.試料・情報の管理について
京都大学血液・腫瘍内科データセンターにおけるデータセットは各研究が終了した後も毎年1回のアップデートを繰り返しながら長期的に保存されます。各研究が論文や学位等研究成果発表の基となった場合は、主研究者においても、当該研究成果発表後10年間、原則電子データとして保存を行います。
あなたの診療情報は、日本造血細胞移植データセンターにてデータを収集する時点で住所、氏名などの個人情報を削除し代わりに新しく番号(匿名化番号)がつけられます。あなたとこの番号とを結びつける対応表は、造血幹細胞移植を受けられた病院で個人情報の管理担当医によって厳重に保管されるため、解析を行う研究者が個人情報を知り得ることはありません。
試料・情報などの二次利用及び他機関への提供の可能性はありますが、その場合は、あらためて研究計画書を作成し、倫理委員会で審議、承認された場合のみ認められます。
6.研究組織
<研究責任者>
京都大学医学部附属病院 血液内科 水本智咲
<共同研究者>
京都大学大学院医学研究科 血液・腫瘍内科 髙折晃史
京都大学大学院医学研究科 血液・腫瘍内科学 近藤忠一
京都大学大学院医学研究科 血液・腫瘍内科学 諫田淳也
京都大学大学院医学研究科 血液・腫瘍内科学 進藤岳郎
京都大学医学部附属病院 検査部・細胞療法センター 新井康之
京都大学医学部附属病院 検査部・細胞療法センター 城 友泰
京都大学医学部附属病院 血液内科 島津 裕
京都大学大学院医学研究科 血液・腫瘍内科学 岩﨑 惇
京都大学大学院医学研究科 血液・腫瘍内科学 渡邊瑞希
京都大学大学院医学研究科 血液・腫瘍内科学 和田典也
京都大学大学院医学研究科 血液・腫瘍内科学 家村知樹
京都大学大学院医学研究科 血液・腫瘍内科学 森田真梨
京都大学大学院医学研究科 血液・腫瘍内科学 林 裕美
京都大学大学院医学研究科 血液・腫瘍内科学 田矢知大
京都市立病院 血液内科 伊藤 満
天理よろづ相談所病院 血液内科 大野仁嗣
天理よろづ相談所病院 血液内科 赤坂尚司
神戸市立医療センター中央市民病院 血液内科 石川隆之
関西電力病院 血液内科 平田大二
関西電力病院 血液内科 和泉清隆
大津赤十字病院 血液免疫内科 竹岡友晴
滋賀県立総合病院 血液・腫瘍内科 浅越康助
兵庫県立尼崎総合医療センター 血液内科 渡邊光正
大阪赤十字病院 血液内科 今田和典
小倉記念病院 血液内科 米澤昭仁
北野病院 血液内科 北野俊行
北野病院 血液内科 坂本宗一郎
倉敷中央病院 血液内科 血液治療センター 上田恭典
倉敷中央病院 血液内科 血液治療センター 前田 猛
静岡県立総合病院 血液内科 野吾和宏
神鋼記念病院 血液内科 有馬靖佳
京都桂病院 血液内科 菱澤方勝
日本赤十字社和歌山医療センター 血液内科 直川匡晴
高槻赤十字病院 血液内科 安齋尚之
高槻赤十字病院 血液内科 恩田佳幸
静岡がんセンター 血液・幹細胞移植科 池田宇次
神戸大学大学院医学研究科小児科学分野 造血幹細胞医療創成学部門 宮西正憲
ネクスジェン株式会社 中島正和
ネクスジェン株式会社 宮塚功
<試料情報管理責任者>
京都大学医学部附属病院 血液内科 水本智咲
7.利益相反について
京都大学では、公的機関だけでなく、一般の企業や財団からも研究資金等の提供を受けて臨床研究を実施しています。また、本学では社会貢献活動の一環として兼業等の活動が認められており、臨床研究に関係する企業・財団との間に個人的な利害関係が生じている研究者もいます。
本研究は京都大学と国立研究開発法人日本医療研究開発機構の事業を実施しているネクスジェン株式会社との再委託研究開発契約にもとづく研究費により実施します。
なお、京都大学においては、ネクスジェン株式会社と特許の共同出願中である髙折晃史と諫田淳也が本研究に関与しています。
京都大学における利益相反については、「京都大学利益相反ポリシー」「京都大学利益相反マネジメント規程」に従い、「京都大学臨床研究利益相反審査委員会」において適切に審査しています。
8.お問い合わせ先
本研究に関するご質問等がありましたら担当医もしくは下記の連絡先までお問い合わせ下さい。
ご希望があれば、他の研究対象者の個人情報及び知的財産の保護に支障がない範囲内で、研究計画書及び関連資料を閲覧することが出来ますのでお申出下さい。
また、情報が当該研究に用いられることについて患者さんもしくは患者さんの代理人の方にご了承いただけない場合には研究対象としませんので、担当医もしくは下記の連絡先までお申出ください。その場合でも患者さんに不利益が生じることはありません。
- 神鋼記念病院代表(電話078-261-6711)
- 京都大学医学部附属病院 血液内科
水本智咲
Tel:075-751-3150, Fax:075-751-3201 - 京都大学医学部附属病院 臨床研究相談窓口
Tel: 075-751-4748 E-mail: ctsodan@kuhp.kyoto-u.ac.jp
再発・難治性FLT3変異陽性急性骨髄性白血病の患者さんに対するギルテリチニブの安全性・有効性の検討
神鋼記念病院血液内科の患者さんへ
2022年8月 神鋼記念病院血液内科
1.研究の目的・意義
ギルテリチニブは,FLT3遺伝子変異陽性の再発又は難治性急性骨髄性白血病に対する治療薬ですが,その有効性及び安全性の情報は限られています。本研究では,実臨床でのギルテリチニブの効果や安全性を調べることを目的とします。
2.情報の取得期間
2020年3月1日から2021年12月31日の間にFLT3遺伝子変異陽性の再発又は難治性急性骨髄性白血病と診断され、ギルテリチニブで治療をうけた患者さんを対象といたします。
3.診療情報の項目
ギルテリチニブの使用状況を含めた臨床情報(年齢,性別,疾患,治療経過など)について,診療録をもとに匿名化した状態で、解析に用います。
4.解析結果は学会発表、論文として公表いたします。
5.個人情報の保護
この研究で得た情報は厳重に管理され、学術目的のみで利用されます。従って、学会発表や論文から個人が特定される恐れはありません。本研究参加者以外の第三者に個人情報が流出することもありません。各患者さんのプライバシーは厳重に保護されますのでご安心ください。
6.利益相反
私共の研究に関して、個人や会社との利益相反はありません。
7.研究への参加を拒否される場合は、当院の下記担当者までご連絡ください。
当院における連絡先: 神鋼記念病院 血液内科/血液病センター
〒651-0072 神戸市中央区脇浜町1丁目4-47
Tel: 078-261-6711、FAX: 078-261-6726
血液内科科長: 常峰紘子
慢性咳嗽・喘息・COPD患者の治療やコントロール状況の調査および各種臨床指標と将来のリスクの関連の検討
研究課題名
慢性咳嗽・喘息・COPD患者の治療やコントロール状況の調査および各種臨床指標と将来のリスクの関連の検討
本件は「オプトアウト」すなわち,同意不要であった既存データを用いた研究において、「自分のデータは使わないでほしい」という、患者さんの拒否の機会を確保するため、研究の公開をホームページ上で行っているものです。今回の研究に該当されることが予想され、「自分のデータは使わないでほしい」と希望される方はご本人・ご家族より当院に手紙、メール、お電話もしくはファックスなどにてその旨ご連絡ください。
神鋼記念病院呼吸器内科に通院中の慢性咳嗽・喘息・COPDの患者さんへ
実施する臨床研究
慢性咳嗽・喘息・COPD患者のコントロール状況の調査および増悪、呼吸機能低下などの将来のリスクに関する臨床研究を実施しております。この研究は「観察研究」と呼ばれるもので、通常の診療で得られた記録をまとめることによって行います。以下の点をご理解いただき、ご協力いただきますようお願い申し上げます。
この研究の意義、目的、および方法
喘息やCOPDなどの慢性気道疾患の管理目標は、症状やQOLの改善などの現状の改善に加え、呼吸機能の低下や増悪などの将来のリスクを低減することが重視されています。日常の外来においても症状や病態の正確な評価を通して将来のリスク低減をもたらすことを目標としております。本研究は当院において日常臨床で行われている各種評価(身体所見、採血、呼吸機能、FENO検査、画像検査、ACTやCATなどの各種問診票および治療内容など)による病態やコントロール状況を評価し、増悪や呼吸機能の変化、合併症との関連などを調査します。患者さんの背景は地域や施設毎に異なるため、より実臨床に即した慢性咳嗽・喘息・COPDの管理に役立てることを目的とします。
この研究による医学上の貢献と予測
日常臨床で得られる情報を通して、現在のコントロール状況を評価し、将来のコントロール向上やリスク低減をもたらす適切な管理ができているかを調査、今後の最適な管理方法を検討します。
この研究による患者さんの不利益および危険性
患者さんの診療情報を分析する研究であり、プライバシーも厳重に保護されますので、患者さんに不利益や危険性はありません。
費用や追加の検査
通常の保険診療による画像診断情報と臨床情報の収集と分析ですので、患者さんに余分な費用を負担してもらうことはありません。また、検査方法の変更や追加検査もありません。
個人情報の保護
この研究で得た情報は厳重に管理され、学術目的のみで利用されます。研究結果は主として統計として処理・解析され発表されるため、個人を特定できることはありません。研究結果の発表に際して、一部の患者さんの臨床情報が参考所見として呈示される可能性がありますが、 匿名化されていますので、個人を特定できることはありません。本研究参加者以外の第三者に流出することもありません。以上のように、患者さんのプライバシーは厳重に保護されますのでご安心ください。
ご協力の拒否について
この研究にご自分のデータが使用されることを拒否される場合は、担当医もしくは下記の問い合わせ先に連絡下さい。たとえ、協力を拒否されても、今後の診療の不利益になることはありません。しかし、拒否のお申し出のあった時点で、既に研究結果が論文などで公表されていた場合には、研究結果を破棄できないことがあります。この場合でも個人が特定されることはありませんので個人情報は保護されます。
研究責任者
神鋼記念病院 呼吸器内科 大塚 浩二郎
当院における連絡先
神鋼記念病院 呼吸器内科 大塚 浩二郎
〒651-0072 神戸市中央区脇浜町1丁目4-47
TEL:078-261-6711 ・ FAX:078-261-6931
特発性好酸球増加症候群において多施設共同研究の既存試料と既存資料を利用し病態関連バイオマーカーを探索する観察研究
はじめに
神鋼記念会 総合健康管理センターでは、過去に神戸大学を中心とする多施設共同研究において、相談または参加された好酸球増加症の患者さんの既存検体や資料を利用して原因不明の好酸球増加症である特発性好酸球増加症候群の診断や治療の選択に役立てようとする研究を実施しております。内容については下記のとおりとなっております。
内容については下記のとおりとなっております。
尚、この研究についてご質問等ございましたら、最後に記載しております[問い合わせ窓口]までご連絡ください。
1. 研究概要および利用目的
特発性好酸球増加症候群は慢性的に白血球中の好酸球細胞が末梢血中に増加し、そのために様々な臓器障害をきたす原因が不明な病気です。この病気の性質や治療の反応性を予測するための研究が2005年から2021年3月まで神戸大学を中心とした全国多施設共同研究として行われ、全国の様々な好酸球増加症の患者さんから末梢血を用いた遺伝子検査の残余検体や病気の情報が収集されました。これまでの活動から、日本人の原因不明の好酸球増加症の患者さんの1-2割にはイマチニブという治療薬が有効な遺伝子異常があることがわかっています。しかし、他の患者さんでは未だに病気の原因となる異常が見つかっていません。この病気の原因は複数である可能性が考えられ、病気の解明には長期間にわたる研究の継続が必要です。今まで神戸大学で研究を中心に行ってきた本研究の代表者がこのたび当センターへ異動するにあたり、2005年2月から2021年3月31日までのあいだに神戸大学に保存された末梢血の残余検体と病気に関する資料を再利用することにより、当センターを中心として特発性好酸球増多症候群の診断や治療に関する研究を開始することといたしました。
2. 研究期間
この研究は、病院長による研究実施許可日から2027年3月31日まで行う予定です。
3. 研究に用いる試料・情報の種類
- 患者基本情報:年齢、性別、診断名、臓器障害の有無、治療方法。
- 一般的な血液検査(白血球数、好酸球数)と生化学検査 (IgE値、VitB12値、TARC値) の結果。
- 染色体検査や遺伝子解析検査が行われた場合はその結果
- 末梢血検体処理の際の白血球細胞収穫量
- PCRアレイ法による好酸球増加症患者11名の遺伝子発現量測定データ
- リン酸化プロテオームによる好酸球増加症患者60名のリン酸化ペプチド解析データ
4. 研究機関
この研究は以下の研究機関のもとで実施いたします。
研究機関
神鋼記念会 総合健康管理センター(研究責任者:定 明子、分担研究者:西川 晋史)
5. 試料・情報の他機関からの取得
本研究では神戸大学医学部附属病院の協力のもと神戸大学大学院医学研究科に保存された既存試料・情報を利用します。
6. 個人情報の管理方法
プライバシーの保護に配慮するため、患者さんの試料や情報は直ちに識別することがすることができないように作成された対応表は引き続き神戸大学大学院医学研究科において管理されます。当センターへのデータ取得は患者さんを直ちに識別できる情報を除く研究に必要な部分を電子媒体で複製し、特定の関係者以外がアクセスできない状態で行います。また、既存試料を用いた新たな測定は研究代表者により主に神戸大学内の実験施設の機器を用いて行われ、残余試料は元の場所に保存されます。
7. 試料・情報等の保存・管理責任者
この研究の試料や情報を保存・管理する責任者は以下のとおりです。
本研究に関連し取得されたデータおよび研究に使用後の残余試料の保存
神鋼記念会 総合健康管理センター(責任者:定 明子)
8. 研究へのデータ提供による利益・不利益
利益・・・・本研究にデータをご提供いただく事で生じる個人の利益は、特にありません。
不利益・・・既存資料・既存試料の使用のみであるため、特にありません。
9. 研究終了後のデータの取り扱いについて
この研究で取得した患者さんの診療に関する情報や本研究開始後に実験により得られた測定データは、論文等の発表から10年間は保管され、その後は患者さんを識別する情報を復元不可能な状態にして破棄されます。また、患者さんが本研究に関するデータ使用の取り止めを申出された際、申出の時点で本研究に関わる情報は復元不可能な状態で破棄いたします。
10. 研究成果の公表について
研究成果が学術目的のために論文や学会で公表されることがありますが、その場合には、患者さんを特定できる情報は利用しません。
11. 研究へのデータ使用の取り止めについて
いつでも可能です。取りやめを希望されたからといって、何ら不利益を受けることはありませんので、データを本研究に用いられたくない場合には、下記の[問い合わせ窓口]までご連絡ください。取り止めの希望を受けた場合、それ以降、患者さんのデータを本研究に用いないようにします。しかしながら、同意を取り消した時、すでに研究成果が論文などで公表されていた場合などのように結果を廃棄できない場合もあります。
12. 問い合わせ窓口
この研究についてのご質問だけでなく、ご自身のデータが本研究に用いられているかどうかをお知りになりたい場合や、ご自身のデータの使用を望まれない場合など、この研究に関することは、どうぞ下記の窓口までお問い合わせ下さい。ご希望があれば、他の研究対象者の個人情報及び知的財産の保護に支障がない範囲内で、研究計画書及び関連資料を閲覧することが出来ますのでお申出下さい。
照会先および研究への利用を拒否する場合の連絡先:
研究責任者:
神鋼記念会 総合健康管理センター 担当者:定 明子
兵庫県神戸市中央区脇浜町1-4-47
電話番号:078-261-6711 (代表)
E-mail:sada.akiko@shinkohp.or.jp
「日本病理剖検輯報(しゅうほう)に基づく全身性アミロイドーシス各病型頻度の疫学調査」ご協力へのお願い
2017年1月1日~2018年12月31日までに病理解剖をされた患者様のご遺族様へ
厚労省アミロイドーシスに関する調査研究班(研究代表者:内木宏延)では、福井大学医学系研究倫理審査委員会の承認および医学系部門長の許可を得て、下記の医学研究を実施しています。
こうした研究では、対象となる方に関して既に存在する試料や情報、あるいは今後の情報や記録などを調査しますが、対象となる方にとって新たな負担や制限が加わることは一切ありません。
このような研究では、国が定めた倫理指針に基づき、対象となる方お一人ずつから直接同意を得るかわりに、研究の目的を含む研究の実施についての情報を公開することが必要とされています。
ご自身の情報や試料を研究に使用してほしくないという場合や利用目的の詳細など研究に関するお問い合わせなどがある場合は、以下の「問い合わせ窓口」へご照会ください。研究への参加を希望されない場合、研究結果の公表前であれば、研究期間内にご連絡いただいた時点より対象から除外いたします。なお研究不参加を申し出られた場合でも、なんら不利益を受けることはありませんのでご安心ください。
福井大学医学部病因病態医学講座分子病理学分野
研究課題名
日本病理剖検輯報(しゅうほう)に基づく全身性アミロイドーシス各病型頻度の疫学調査
研究期間
2021年4月8日~2024年3月31日
研究の意義・目的
全国の病理施設で1年間に行われた剖検症例の診断をまとめた日本病理剖検輯報(しゅうほう)(日本病理学会編)を用いて、国内で1 年間にアミロイドーシスと報告された症例を抽出することができます。
本研究では、2017年1月1日~2018年12月31日までにアミロイドーシスと報告された症例に関して、各施設にアンケート調査を実施すると共に、福井大学にて追加の検査を行い、各病型を正確に決定し、日本の剖検例におけるアミロイドーシス各病型の疫学調査を行うことを目的としています。
研究の内容
1.研究の対象となる方
2017年1月1日~2018年12月31日までに病理解剖が施行され、アミロイドーシスと報告された患者様
2.研究に用いる試料・情報
- 日本病理剖検輯報に記載されている事項(患者年齢、性、臨床診断、病理解剖診断、主な治療)
- 検体から同定したアミロイド蛋白質の種類
なお、研究成果は学会や雑誌等で発表されますが、個人を識別できる情報は削除し、公表しません。また、取り扱う試料・情報は厳密に管理し、漏洩することはありません。
3.研究の方法
日本病理剖検輯報(しゅうほう)第60 輯 (2019 年刊行)~第61 輯 (2020 年刊行) を対象とします。
輯報(しゅうほう)に添付されたCD-ROM 中のpdf 版をエクセル化し、キーワード検索によりアミロイドーシス症例を抽出します。
病型に関する情報が不確実な症例は、登録施設に簡潔なアンケート調査を実施し、病型を確定します。
アンケート調査によっても病型を確定できない場合、登録施設より臓器の未染色標本を送付していただき、アミロイドーシスに関する調査研究班の病型診断コンサルテーションシステムによるパネル染色により病型を確定します。パネル染色により病型を確定できなかった症例は、熊本大学大学院生命科学研究部(共同研究機関)に送り、アミロイド前駆蛋白質の質量分析 LMD/LC-MS/MS による同定を行います。
データの提供は、特定の関係者以外が閲覧できない状態で郵送によって行います。対応表は、本学の研究責任者が保管・管理します。
得られたデータを基に、全身性アミロイドーシス各病型の日本における精確な発症頻度等を明らかにし、論文での発表を通して、日本における全身性アミロイドーシスの疫学的な実態を明らかにします。
利益相反について
利益相反とは、外部との経済的な利益関係(資金提供など)によって、研究データの改ざん、特定企業の優遇など研究が公正かつ適切に行われていないのではないか(企業に有利な結果しか公表されないのではないか)と第三者から懸念されかねない事態のことをいいます。
この研究は、特定の企業や団体から研究資金や給与・謝金など、特別な便宜を受けていないことを福井大学臨床研究利益相反審査委員会に全て報告し、利益相反状態でないと判定されています。研究を公正に遂行し、対象となる方に不利益になることや、研究結果を歪めることは一切いたしません。
研究計画書及び研究の方法に関する資料の入手・閲覧方法
本研究では、研究計画書及び研究の方法に関する資料に関しては、他の研究対象者等の個人情報及び知的財産の保護等に支障がない範囲内に限り入手又は閲覧が可能です。その入手・閲覧をご希望される際には下記「問い合わせ先」までご連絡下さい。
個人情報の開示等に関する手続き
本学が保有する個人情報のうち、本人の情報について、開示、訂正及び利用停止を請求することができます。詳しくは下記ホームページをご覧ください。
≪福井大学における個人情報保護について≫
http://www.u-fukui.ac.jp/cont_about/disclosure/privacy/
研究責任者
福井大学医学部病因病態医学講座分子病理学分野
教授 内木 宏延
研究分担者
福井大学医学部病因病態医学講座分子病理学分野
山口 愛奈
共同研究機関
熊本大学大学院生命科学研究部
教授 植田 光晴
研究事務局(連絡・問い合わせ先)
〒910-1193 福井県吉田郡永平寺町松岡下合月23-3
福井大学医学部病因病態医学講座分子病理学分野
岡田 ひろみ
電話:0776-61-3111(内線2237)
FAX:0776-61-8123
E-mail:amyloid@med.u-fukui.ac.jp
ご意見・苦情窓口
〒910-1193
福井県吉田郡永平寺町松岡下合月23-3
福井大学医学部附属病院医学研究支援センター
電話:0776-61-8529
受付時間:平日8:30~17:15(年末年始、祝・祭日除く)
間質性肺炎に対する抗線維化薬ニンテダニブ・ピルフェニドン投与が肺血行動態に与える影響評価
患者さんへ
はじめに
神鋼記念病院と協力候補機関では、2015年4月1日から2025年3月31日の期間中に入院または外来において、間質性肺炎の診断を受けられた患者さんを対象に研究を実施しております。内容については下記のとおりとなっております。
尚、この研究についてご質問等ございましたら、最後に記載しております[問い合わせ窓口]までご連絡ください。
1. 研究の意義および目的
間質性肺炎のある患者様はしばしば肺高血圧症を合併することが知られていますが、肺高血圧症を合併すると予後が悪化する可能性が指摘されています。特発性肺線維症を含む進行性の間質性肺炎に対しては、線維化抑制効果を有するピルフェニドンやニンテダニブの内服がすすめられることがあります。その一方で、もともと酸素投与を必要とする患者様においては、抗線維化薬ニンテダニブが肺高血圧の合併に関与するのではないか、と注意を投げかける報告があります。しかしながらもう一つの抗線維化薬ピルフェニドンも含め、本当に肺高血圧の発症や悪化に関与するかどうかははっきりしていません。
この度、間質性肺炎に対する抗線維化薬が肺高血圧の発症・悪化に関与するのかどうかの検証と、もし関与する場合にはどのような患者様が増悪しやすいのか、さらには肺高血圧の悪化が実際の症状や予後に関与するのかを明らかにするために、本研究を開始し、今後の間質性肺炎診療の発展に貢献したいと考えております。そのために、抗線維化薬を内服する患者さんと内服しない患者様の肺高血圧に関する心エコー・右心カテーテルの情報や肺高血圧以外に関する情報を比較し、解析する予定です。
2. 研究期間
この研究は、2015年4月1日から2025年3月31日までの症例を解析予定です。
3. 取り扱うデータ
患者背景(性別、年齢、身長、体重、既往症、使用中の薬剤)、血液検査、動脈血液ガス検査、心エコー、右心カテーテル検査、WHO機能クラス、運動機能(6分間歩行距離)、呼吸機能検査、胸部レントゲン、胸部CT、健康関連QOL(生活の質)尺度、ADL(日常生活動作)指標 等
抗線維化薬を内服する患者さんと内服しない患者様の肺高血圧に関する心エコー・右心カテーテルの情報や肺高血圧以外に関する情報を比較し、解析する予定です。
4. 個人情報保護の方法
個人情報、検査結果などの記録、保管は第三者が直接患者さんを識別できないよう登録時に定めた登録番号を用いて行います。また得られた記録は、インターネットに接続していない外部記憶装置に記録し、各肺高血圧診療施設の鍵のかかる保管庫に保管します。
5. 研究へのデータ提供による利益・不利益
- 利益……将来的に間質性肺炎の治療の進歩に貢献いただける可能性がありますが、本研究中にデータをご提供いただいた患者さん個人の治療に利益は生まれません。右心カテーテル検査については、肺高血圧症を合併してくる患者さんにより早期に気付ける可能性があります。
- 不利益……通常診療の範囲内で施行するため、特にありません。研究に同意いただいた時点で抗線維化薬を内服しない方針であったとしても、その後あなたの間質性肺炎の病状をみて担当医が抗線維化薬の内服開始したほうがよいと考えた場合、内服を開始いただくことができます。また一方の抗線維化薬の副作用が強く出た場合などに、担当医が薬剤を中止したり、もう一方の抗線維化薬に変更したりほうがよい、と判断すれば変更や中止も可能です。そのため間質性肺炎の従来の診療以上の不利益は生じません。右心カテーテル検査については、肘や首、鼠径部の静脈から行いますが、まれに検査中に腕の痛み、脈拍の乱れ、内出血などが起こりえます。また2日以上の入院が必要となります。詳しくは右心カテーテル検査の同意書をご覧ください。健康関連QOLの質問票チェックには5~10分程度いただきます。
6. 研究終了後のデータの取り扱いについて
この研究で取得した患者さんの治療に関する情報は、論文等の発表から10年間は保管され、その後は患者さんを識別する情報を復元不可能な状態にして破棄されます。また、患者さんが本研究に関するデータ使用の取り止めを申出された際、申出の時点で本研究に関わる情報は復元不可能な状態で破棄いたします。
7. 研究成果の公表について
研究成果が学術目的のために論文や学会で公表されることがありますが、その場合も、患者さんの個人情報の秘密は厳重に守られますので、第三者に患者さんの個人情報が明らかになることはありません。
8. 研究へのデータ使用の取り止めについて
いつでも可能です。取りやめを希望されたからといって、何ら不利益を受けることはありませんので、データを本研究に用いられたくない場合には、下記[問い合わせ窓口]までご連絡ください。取り止めの希望を受けた場合、それ以降、患者さんのデータを本研究に用いることはありません。しかしながら、すでに研究成果が論文などで公表されていた場合のように、結果を廃棄できない場合もあります。
9. 研究機関
この研究は以下の研究機関で実施いたします。
代表研究機関:神鋼記念病院
(研究責任者:循環器内科 中山 和彦 研究担当者:呼吸器内科 稲尾 崇)
協力研究機関:随時追加
10. 問い合わせ窓口
この研究についてのご質問だけでなく、ご自身のデータが本研究に用いられているかどうかをお知りになりたい場合や、ご自身のデータの使用を望まれない場合など、この研究に関することは、どうぞ下記の窓口までお問い合わせ下さい。
代表研究機関:神鋼記念病院
研究担当者:神鋼記念病院 呼吸器内科 稲尾 崇
代表研究機関:神鋼記念病院
住所:〒651-0072 神戸市中央区脇浜町1丁目4-47
TEL:078-261-6711・FAX:078-261-6726
コロナウィルス肺炎(CoVP)とインフルエンザウィルス肺炎(InVP)、非ウィルス性市中肺炎(nVCAP)の臨床像に関する多施設共同研究のお知らせ
研究の背景と目的
私たちはコロナウィルス肺炎の病態をインフルエンザウィルス肺炎や非ウィルス性市中肺炎と比較する研究を行っています。市中肺炎とは、医療関連行為を受けていない方に家庭で起こった肺炎です。2019年中国武漢に端を発したコロナウィルスによる肺炎は世界的な拡大をみせつつあります。現在あるコロナウィルス肺炎のデータの多くは中国での記録によるものですが、 一般的なウィルス性肺炎の性質を示したものも多く、 コロナウィルス以外のウィルス性肺炎(これまでの日本では多くはインフルエンザウィルス肺炎になります)や非ウィルス性の市中肺炎との比較はなされておらずその臨床的特徴・違いは明らかではありません。そこで、京都大学および関連の病院に入院されたコロナウィルス肺炎もしくはインフルエンザウィルス肺炎や非ウィルス性市中肺炎の患者さんを多人数集積して、コロナウィルス肺炎の診療に役立つ情報や日本のコロナウィルス肺炎の特徴を見出すことを目的としました。
対象となる患者さんと方法
この研究は、倫理委員会での承認から2年間までにNPO法人 西日本呼吸器内科医療推進機構の研究参加病院に入院され、コロナウィルス肺炎として治療を受けられた(または、治療を受けられる)患者さんを対象として登録し、患者さんのカルテを閲覧し、病状や基礎疾患、検査データ、画像所見、原因病原体、治療効果などのデータを解析するものです。解析の期間も含めた研究実施期間は5年間を予定しています。カルテの閲覧は医師が行い、カルテが施設外に持ち出されることはありません。調査には患者さんのお名前は使用せず、番号で管理されますので、個人情報(お名前や住所など個人が特定できる情報)は保護されます。入院時の年齢、性別、体温や採血の結果、また最終的な転帰などをデータとして京都大学呼吸器内科において管理します。
拒否の希望のある患者さんへ
本研究は京都大学大学院医学研究科・医学部及び医学部附属病院 医の倫理委員会の審査を受け、研究機関の長の許可を受けて実施しているものですが、対象となる患者さんにつきましては、ご異存がなければ調査に加えさせていただきたくお願いします。もしそれを望まれない場合やご質問がある場合は下記までご連絡ください。ご協力いただけない場合でも、今後の診療に不利益はきたしません。なお、研究結果は、学会や出版物として公表することがあります。
研究資金と利益相反
研究資金は京都大学呼吸器内科の研究費によって賄われ、企業との利益相反はありません。利益相反については、「京都大学利益相反ポリシー」「京都大学利益相反マネジメント規程」に従い、「京都大学臨床研究利益相反審査委員会」において適切に審査・管理もされます。
ご理解とご協力のほど、どうぞよろしくお願いいたします。
予定共同研究機関(各病院に直接問い合わせることはお控えください)
明石医療センター呼吸器内科、部長 大西尚
赤穂市民病院内科、医師 村瀬公彦
大阪赤十字病院呼吸器内科、部長 西坂奏夫
大阪府済生会中津病院呼吸器内科、部長 長谷川吉則
大津赤十字病院呼吸器内科、部長 酒井直樹
岸和田市民病院呼吸器内科、部長 高橋憲一
京都市立病院呼吸器内科、部長 江村正仁
京都南病院呼吸器内科、副院長 新林成介
倉敷中央病院呼吸器内科、部長 石田直
神戸市立医療センター中央市民病院呼吸器内科、部長 富井啓介
神戸市立医療センター西市民病院呼吸器内科、部長 冨岡洋海
公立豊岡病院組合立豊岡病院呼吸器内科、医長 中治仁志
国立病院機構姫路医療センター呼吸器内科、部長 河村哲治
堺市立総合医療センター呼吸器内科、部長 郷間厳
静岡市立静岡病院呼吸器内科、 部長 山田孝
新京都南病院呼吸器内科、部長 新林成介
杉田玄白記念公立小浜病院内科、医師 伊藤功朗
田附興風会医学研究所北野病院呼吸器内科、部長 福井基成
天理よろづ相談所病院呼吸器内科、部長 羽白高
市立長浜病院呼吸器内科、部長 野口哲男
西神戸医療センター呼吸器科、部長 多田公英
日本赤十字社和歌山医療センター呼吸器内科、部長 杉田孝和
彦根市立病院呼吸器内科、部長 月野光博
兵庫県立尼崎総合医療センター呼吸器内科、部長 平林正孝
福井赤十字病院呼吸器内科、部長 赤井雅也
洛和会音羽病院呼吸器内科、部長 土谷美知子
高槻赤十字病院呼吸器内科、部長 北英夫
綾部市立病院、医師 濱田哲
神鋼記念病院呼吸器内科、部長 大塚浩二郎
寺田内科・呼吸器科、院長 寺田邦彦
研究責任者
〒606-8507 京都市左京区聖護院川原町54
京都大学医学部附属病院呼吸器内科 伊藤功朗
連絡先:075-751-3830、メール:isaoito@kuhp.kyoto-u.ac.jp
神鋼記念病院の相談窓口
神鋼記念病院 呼吸器内科部長 大塚浩二郎
(Tel)078-261-6711
本研究で収集した試料・情報は、同意を受ける時点では特定されない将来の研究のために用いる可能性があります。他の研究への二次利用および他研究機関へ提供する際は、新たな研究計画について倫理委員会で承認された後に行います。また、ホームページ上で、研究の目的を含む研究実施の情報を公開し、研究対象者が拒否できる機会を保障します。
研究に関するお知らせ
(研究課題名:COVID-19 に関するレジストリ研究)
神鋼記念病院では、以下にご説明する研究を行います。この研究への参加を希望されない場合には、あなたが入院した医療機関または下記のお問い合わせ先にお申し出ください。お申し出になられても、いかなる不利益も受けることはございませんので、ご安心ください。未成年者の方や現在ご自身で研究参加の判断が難しいと考えられる方においては、家族や親族等からの研究不参加のお申し出やお問い合わせに対してもご対応いたします。
研究目的・方法
2019年12月から中国の武漢市で新型コロナウイルスによる肺炎の集団発生が確認されました。この新型コロナウイルス感染症(以下、COVID-19)はその後全世界に拡がり、日本国内でも多くの感染者が報告されています。無症状の方から重症化する方まで症状や重症度は幅広く、また、妊婦や小児などの症例も報告されています。新しいウイルスによる感染症であるため、効果のある治療法に関する情報は限られており、また、どのような方が重症化しやすいかなど、多くのことがまだわかっていません。この研究では、COVID-19と診断された方に参加していただき、重症化する方の特徴や経過、薬剤投与後の経過など、COVID-19に関する様々な点について明らかにするための情報を集めることを目的としています。
研究期間
理事長承認日~西暦2024年3月31日
研究の対象となる方
2020年1月1日以降にCOVID-19と診断され、日本国内の医療機関に入院された方
ご協力頂く内容
上記の対象期間中に記録された診療情報(年齢、性別、発症日や入退院日、基礎疾患・併存疾患、転送歴、生活習慣、出生国、人種、COVID-19の罹患に関わる疫学的情報(職業歴や渡航歴を含む)、内服歴・治療歴、妊娠の有無やその経過 [女性のみ]、身長・体重、以前のCOVID-19感染歴やワクチン接種歴、入院時の症状・徴候や全身状態、薬剤や酸素などその他の治療の状況、合併症、転帰、臨床検査結果(新型コロナウイルスやその他の病原体検査を含む)、臨床画像所見など)を研究に使用させて頂きます。使用に際しては、文部科学省・厚生労働省が定めた倫理指針に則って個人情報を厳重に保護し、研究結果の発表に際しても、個人が特定されない形で行います。
研究参加について
研究への参加を希望されない場合、その方の情報を研究における解析に利用することはありません。ただし、COVID-19は新規の感染症であることから、社会的・公衆衛生的に重要であるため、原則として全ての患者さんの情報をこの研究のデータベースには登録させていただきます。研究に参加される場合でもされない場合でも、患者さん個人を特定できるような情報が外部に漏れることはありません。
新興・再興感染症データバンク事業(REBIND)への情報の提供
本研究に登録された情報は、新興・再興感染症データバンク事業(REBIND)へ提供されます。詳細は別紙「COVID-19に関するレジストリ研究(COVID-19 Registry)にご協力いただいた患者様へ」をご確認ください。
外部への試料・情報の提供
研究データの提供は、特定の関係者以外がアクセスできない状態で行います。提供されるデータと該当する患者さんを記録しておく匿名化対応表は、該当する患者さんが診療を受けた病院の研究責任者や個人情報管理者などが保管・管理します。研究のデータは、WHOなどの国際的な研究グループと共有する場合があります。その場合、匿名化対応表は提供せず、個人の特定ができない状態で共有します。また、社会的意義がある等の理由で本研究データ利用のための審議で認められた場合のみ、研究データを企業等が利用する可能性があります。この場合も個人の特定はできません。
研究組織
研究代表機関: 国立研究開発法人国立国際医療研究センター 大曲 貴夫
情報提供機関: COVID-19の方を診療した国内全ての医療機関
利益相反について
利益相反の状況は、研究代表機関においてはNCGM利益相反マネジメント委員会に報告し、その指示を受けて適切に管理します。共同研究機関においてはそれぞれの機関のルールにのっとって適切に報告・管理されます。本研究に関する研究全体及び研究者個人として申告すべき利益相反の状態はありません。
研究計画書等の入手・閲覧方法・手続き等
あなたのご希望により、この研究に参加してくださった方々の個人情報の保護や、この研究の独創性確保に支障がない範囲で、この研究の計画書や研究の方法に関する資料、研究成果の一部などをご覧いただくことができます。以下のURLからご確認ください。
https://covid-registry.ncgm.go.jp/general/
個人情報の開示に係る手続きについて
本研究で収集させて頂いたご自身の情報を各医療機関の規定に則った形でご覧頂くことも出来ます。ご希望される方は、COVID-19のために受診した医療機関にお申し出ください。
当院の研究責任者・本研究全体の研究代表者:
国立研究開発法人国立国際医療研究センター 国際感染症センター 大曲 貴夫
お問い合わせ先
神戸市中央区脇浜町1丁目4-47
社会医療法人神鋼記念会 神鋼記念病院
研究担当医師:呼吸器内科 大塚浩二郎
078-261-6711(代表) (月~金 8:30~17:15)
「前立腺癌患者におけるアビラテロン併用アンドロゲン遮断療法が骨量に与える影響の観察研究」について
(当院は、神戸大学の共同研究施設として参加しています)
はじめに
神戸大学大学院医学研究科 外科系講座 腎泌尿器科学分野では、2019年11月1日から2021年10月31日までの間に前立腺癌に対しアビラテロン併用アンドロゲン遮断療法を開始した患者さんを対象に研究を実施しております。内容については下記のとおりとなっております。
尚、この研究についてご質問等ございましたら、最後に記載しております[問い合わせ窓口]までご連絡ください。
研究概要および利用目的
神戸大学大学院医学研究科 外科系講座 腎泌尿器科学分野では、前立腺癌患者さんに対しアビラテロン併用アンドロゲン遮断療法を行っております。
アンドロゲン遮断療法は骨密度が低下する副作用があると言われており、低下した場合の早期発見・早期治療が推奨されています。そのため、神戸大学大学院医学研究科 外科系講座 腎泌尿器科学分野でも、アンドロゲン遮断療法を受けておられる患者様には定期的に採血やレントゲンを行なっています。また、アビラテロンと併用するステロイド(プレドニゾロン)にも骨粗鬆症を引き起こす副作用があると言われています。以上から、アビラテロン併用アンドロゲン遮断療法は、理論的には骨粗鬆症を引き起こすリスクの高い治療と考えられますが、実際どの程度骨粗鬆症が起こりうるのかを調べた研究は今のところありません。
そこで今回、アビラテロン併用アンドロゲン遮断療法施行中の骨粗鬆症や骨折の頻度を調査することにしました。
研究期間
この研究は、倫理委員会承認日から2025年3月31日まで行う予定です。
研究に用いる試料・情報の種類
- 基本情報:年齢、performance status、既往歴、治療開始前PSA値、臨床ステージ、骨転移の有無、診断時Gleason score、既往歴
- 治療内容:過去の放射線治療併用の有無、手術療法併用の有無
- 検査結果:ホルモン治療開始前/開始12ヶ月/24ヶ月/36ヶ月の骨関連マーカー(骨型アルカリフォスファターゼ、酒石酸耐性酸性ホスファターゼ、5b1型プロコラーゲン-N-ペプチド)、若年成人比較%(YAM値、大腿骨近位部、腰椎)大腿骨近位部、腰椎)
- 検査結果:開始6ヶ月/18ヶ月/30ヶ月のYAM値(大腿骨近位部、腰椎)
- 骨折の有無:フォロー期間中の骨折の有無、発生時はその年月日
- ホルモン治療開始前/開始12ヶ月/24ヶ月/36ヶ月のQOLアンケート結果
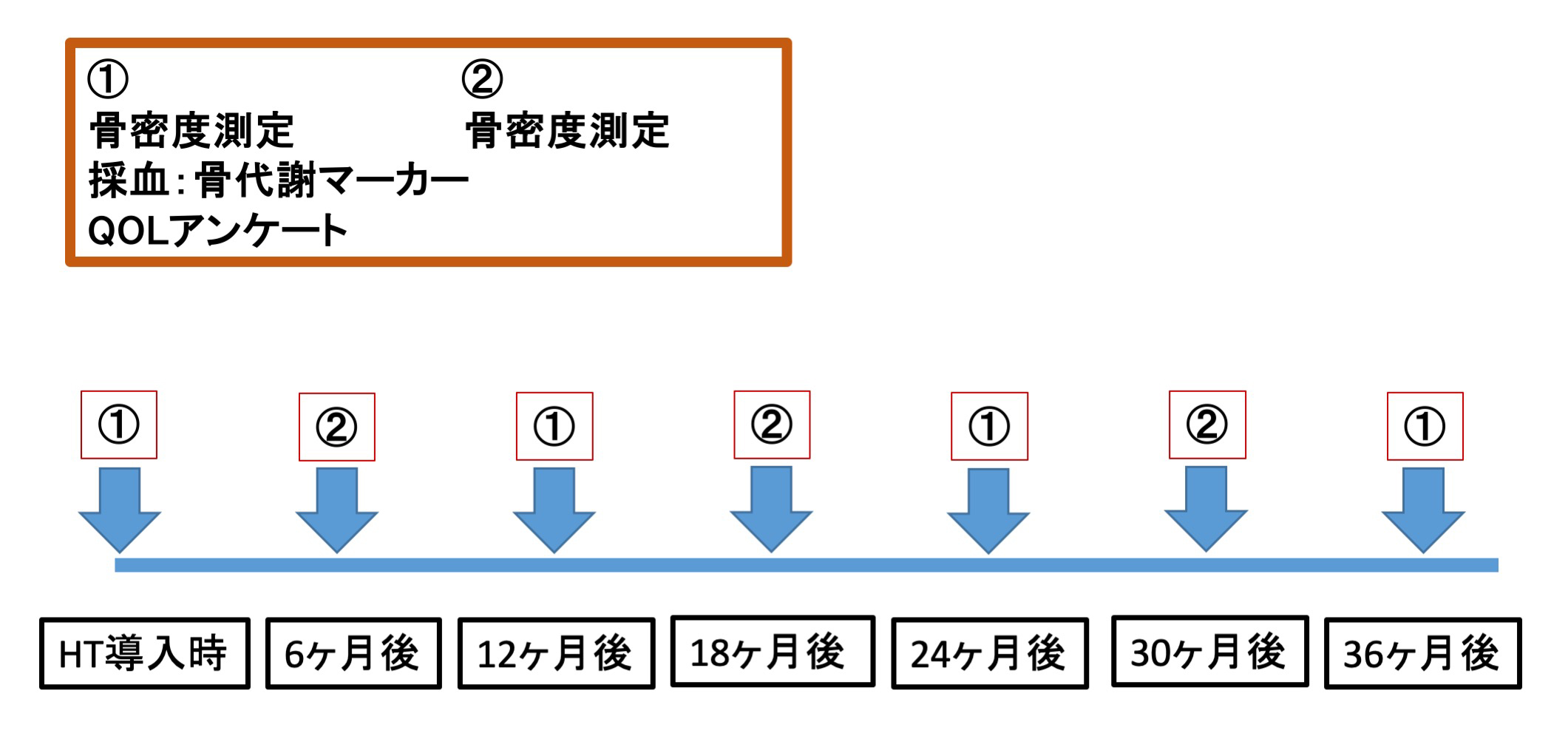
個人情報の管理方法
プライバシーの保護に配慮するため、患者さんの情報は直ちに識別することがすることができないよう、対応表を作成して管理します。収集された情報や記録は、インターネットに接続していない外部記憶装置に記録し、神戸大学大学院医学研究科外科系講座腎泌尿器科学研究室の鍵のかかる保管庫に保管します。
試料・情報等の保存・管理責任者
この研究の試料や情報を保存・管理する責任者は以下のとおりです。
神戸大学大医学部附属病院 泌尿器科 責任者:板東 由加里
研究へのデータ提供による利益・不利益
利益・・・・本研究にデータをご提供いただく事で生じる個人の利益は、特にありません。
不利益・・・カルテからのデータ収集および既存の検体の使用のみであるため、特にありません。
研究終了後のデータの取り扱いについて
患者さんよりご提供いただきました試料や情報は、研究期間中は神戸大学大学院外科系講座腎泌尿器科学分野において厳重に保管いたします。ご提供いただいた試料や情報が今後の医学の発展に伴って、他の病気の診断や治療に新たな重要な情報をもたらす可能性があり、将来そのような研究に使用することがあるため、研究終了後も引き続き神戸大学大学院外科系講座腎泌尿器科学分野で厳重に保管させていただきます。(保管期間は最長で10年間です。)
なお、保存した試料や情報を用いて新たな研究を行う際は、医学倫理委員会の承認を得た後、情報公開文書を作成し病院のホームページに掲載します。
ただし、患者さんが本研究に関するデータ使用の取り止めを申出された場合には、申出の時点で本研究に関わる情報は復元不可能な状態で破棄いたします。
研究成果の公表について
研究成果が学術目的のために論文や学会で公表されることがありますが、その場合には、患者さんを特定できる情報は利用しません。
研究へのデータ使用の取り止めについて
いつでも可能です。取りやめを希望されたからといって、何ら不利益を受けることはありませんので、データを本研究に用いられたくない場合には、下記の[問い合わせ窓口]までご連絡ください。取り止めの希望を受けた場合、それ以降、患者さんのデータを本研究に用いることはありません。しかしながら、同意を取り消した時、すでに研究成果が論文などで公表されていた場合には、結果を廃棄できない場合もあります。
問い合わせ窓口
この研究についてのご質問だけでなく、ご自身のデータが本研究に用いられているかどうかをお知りになりたい場合や、ご自身のデータの使用を望まれない場合など、この研究に関することは、どうぞ下記の窓口までお問い合わせ下さい。ご希望があれば、他の研究対象者の個人情報及び知的財産の保護に支障がない範囲内で、研究計画書及び関連資料を閲覧することが出来ますのでお申出下さい。
照会先および研究への利用を拒否する場合の連絡先:
神戸大学医学部附属病院 泌尿器科 担当者:板東 由加里
神戸市中央区楠町7-5-2
078-382-6155
神鋼記念病院 泌尿器科 担当者:安福 富彦
神戸市中央区脇浜町1丁目4-47
078-261-6711
研究代表者:
神戸大学大学院医学研究科 外科系講座 腎泌尿器科学分野 藤澤 正人
研究責任者
神戸大学医学部附属病院 泌尿器科 藤澤 正人
加古川中央市民病院 泌尿器科 岡 泰彦
関西労災病院 泌尿器科 川端 岳
北播磨総合医療センター 泌尿器科 武市 佳純
甲南医療センター 泌尿器科 田中 浩之
神戸市立医療センター西市民病院 泌尿器科 中村 一郎
神戸赤十字病院 泌尿器科 木下 佳久
三田市民病院 泌尿器科 宮崎 茂典
神鋼記念病院 泌尿器科 山下 真寿男
新須磨病院 泌尿器科 原田 益善
製鉄記念広畑病院 藤井 明
高砂市民病院 泌尿器科 上野 康一
丹波医療センター 泌尿器科 吉村 光司
姫路赤十字病院 泌尿器科 小川 隆義
兵庫県立淡路医療センター 泌尿器科 吉行 一馬
兵庫県立加古川医療センター 泌尿器科 田中 宏和
兵庫県立がんセンター 泌尿器科 井上 隆朗
兵庫県立尼崎総合医療センター 泌尿器科 山田 裕二
淀川キリスト教病院 泌尿器科 前田 浩志
「本邦リアルワールドでの重症喘息における生物学的製剤の使用実態および効果に寄与する因子の検討」について
研究の対象
2009年1月から重症喘息で生物学的製剤の投与をされた方
研究目的・方法
本邦実臨床において重症喘息に対する生物学的製剤の使用実態が明らかとする。これにより、生物学的製剤の適正使用の推進となる基盤となるデータが確立し、解決すべき課題が明らかにされることが期待される。
研究期間:許可日~5年間
研究に用いる試料・情報の種類
通常診療における診療録から抽出された臨床データ(年齢、性別、喫煙歴、肺機能、呼気一酸化窒素、末梢血好酸球数、血清IgE値、診断名、投薬歴、入院歴、呼吸器症状の変化などの経過情報)
外部への試料・情報の提供
データセンターへのデータの提供は、特定の関係者以外がアクセスできない状態で行います。対応表は、当院の研究責任者が保管・管理します。
研究組織
丸毛 聡 公益財団法人田附興風会医学研究所北野病院呼吸器内科部長
福井 基成 公益財団法人田附興風会医学研究所北野病院副院長
北島 尚昌 公益財団法人田附興風会医学研究所北野病院呼吸器内科副部長
白石 祐介 公益財団法人田附興風会医学研究所北野病院呼吸器内科医員
林 優介 公益財団法人田附興風会医学研究所北野病院呼吸器内科レジデント
渡辺 徹也 大阪市立大学大学院医学研究科呼吸器内科学講師
森田 恭平 大阪赤十字病院呼吸器内科医長
豊蔵 恵里佳 大阪赤十字病院呼吸器内科医員
吉村 千恵 大阪赤十字病院呼吸器内科副部長
原永 修作 琉球大学医学部附属病院特命准教授
佐藤 陽子 豊見城中央病院呼吸器内科部長
知花 なおみ 那覇市立病院内科部長
福山 一 森園病院内科医長
松永 和人 山口大学大学院医学系研究科呼吸器・感染症内科学教授
服部 登 広島大学大学院分子内科学教授
時岡 史明 公益財団法人大原記念倉敷中央医療機構倉敷中央病院呼吸器内科部長
立川 良 神戸市立医療センター中央市民病院呼吸器内科医長
大塚 浩二郎 神鋼記念病院呼吸器内科長
中治 仁志 豊岡病院呼吸器内科医長
寺田 邦彦 寺田内科・呼吸器科院長
重松 三知夫 住友病院呼吸器内科部長
上田 哲也 大阪府済生会中津病院呼吸器内科副部長
松本 健 大阪府済生会野江病院呼吸器内科医長
樋上 雄一 市立吹田市民病院呼吸器内科医長
北 英夫 高槻赤十字病院呼吸器内科部長
西田 幸司 堺市立総合医療センター呼吸器内科副部長
山本 傑 大阪南医療センター呼吸器内科部長
寺西 敬 敬任会病院総合内科医長
室 繁郎 奈良県立医科大学呼吸器内科学教授
土屋 美知子 洛和会音羽病院呼吸器センター部長
安場 広高 三菱京都病院呼吸器・アレルギー科顧問
塩田 哲広 滋賀県立総合病院呼吸器内科部長
高橋 珠紀 大津赤十字病院呼吸器内科医長
福家 聡 KKR札幌医療センター呼吸器内科部長代行
南 幸範 旭川医科大学病院呼吸器センター助教
お問い合わせ先
本研究に関するご質問等がありましたら下記の連絡先までお問い合わせ下さい。
ご希望があれば、他の研究対象者の個人情報及び知的財産の保護に支障がない範囲内で、研究計画書及び関連資料を閲覧することが出来ますのでお申出下さい。
また、試料・情報が当該研究に用いられることについて患者さんもしくは患者さんの代理人の方にご了承いただけない場合には研究対象としませんので、下記の連絡先までお申出ください。その場合でも患者さんに不利益が生じることはありません。
照会先および研究への利用を拒否する場合の連絡先:
〒651-0072 神戸市中央区脇浜町1-4-47
社会医療法人神鋼記念会 神鋼記念病院
電話:078-261-6711、FAX:078-261-6931
呼吸器内科 科長 大塚浩二郎
「全国胆道癌の後方視的観察研究」について
研究の対象
2016年1月~2025年12月に当院で胆道癌(肝門部領域胆管癌、遠位胆管癌、胆嚢癌、十二指腸乳頭部癌)と診断された方
研究目的・方法・研究期間
本邦における胆道癌(肝門部領域胆管癌、遠位胆管癌、胆嚢癌、十二指腸乳頭部癌)症例の疫学調査を行うことにより、これを基に胆道癌取扱い規約の改訂とともに国際対癌連合( The Union for International Cancer Control, 略して UICC )が提案した TNM分類と病期分類の検証を行い、胆道癌に関する研究ならびに診療の進歩・知識の普及を図ります。カルテに記載された情報を全国から集めて研究します。研究期間は、2035年12月31日までです。 本研究は日本肝胆膵外科学会の資金で行われており、企業との利益相反はありません。
研究計画書(PDF)
研究に用いる試料・情報の種類
癌の進行度や治療法などのカルテ情報のみを個人が分からないようにして提供します。
外部への試料・情報の提供
データセンターへのデータの提供は、特定の関係者以外がアクセスできない状態で行います。対応表は、当センターの研究責任者が保管・管理します。
研究組織
研究代表者:
藤田医科大学 消化器外科 職名 教授 氏名 堀口明彦
当院の研究責任者:
神鋼記念病院 消化器外科 職名 部長 氏名 藤本 康二
共同研究機関:
日本肝胆膵外科学会胆道癌登録病院 528 機関(藤田医科大学消化器外科ホームページに掲載)
除外の申出・お問い合わせ先
試料・情報が本研究に用いられることについて研究の対象となる方ご了承いただけない場合には、研究対象から除外させていただきます。下記の連絡先までお申し出ください。その場合でも、お申し出により、研究の対象となる方その他に不利益が生じることはありません。 本研究に関するご質問等がありましたら下記の連絡先までお問い合わせ下さい。 また、ご希望があれば、他の研究対象者の個人情報及び知的財産の保護に支障がない範囲内で、研究計画書及び関連資料を閲覧することが出来ますのでお申出下さい。
照会先および研究への利用を拒否する場合の連絡先:
神鋼記念病院 消化器外科
担当者:藤本 康二
兵庫県神戸市中央区脇浜町1-4-47
電話 078-261-6711
「日本整形外科学会症例レジストリー(JOANR)構築に関する研究」について
1. 試料・情報の利⽤⽬的及び利⽤⽅法
A) ⽬的:運動器疾患の⼿術に関する⼤規模データベースの構築
B) ⽅法:⽇本整形外科学会が運営するインターネット上のレジストリシステムへの登録
2. 利⽤⼜は提供する資料・情報の項⽬
A) データベースの1階部分(日整会主導の調査項目):患者ID(匿名化ID①:各データ登録機関のルールにより個人情報保護法に準拠し作成し、対応表で管理する。匿名化ID②:データ登録機関コード+ナンバリング)、年齢、性別、ハッシュ値①(患者氏名<読み>、性別、生年月日、その他の項目より作成→アウトカムとしての再手術時の患者突合に利用)、医療機関コード、疾患情報(標準病名、ICD-10 コード、病名管理番号、病名変換用コード)、手術情報(K コード、入院・外来別)、手術時間、麻酔時間、手術日、術者情報(日整会会員情報と連結)、看護師数、技師数、治療成績(術後30 日におけるアウトカム「改善・不変・悪化・術後30 日以内の再入院」)
B) データベースの2 階部分(関連学会主導の調査項目)
① 人工関節手術
1. ハッシュ値②(患者の出身県、患者名<読み>の最初の一文字を加え作成する)
2. 手術内容(THA、TKA/UKA/PFA、解剖学的TSA/リバース型TSA)
3. 手術概要:
○ 初回手術:手術側、既往手術、手術診断名
○ 再手術:初回手術年月日、初回手術施設名、初回手術診断名、手術側、手術の理由、手術の内容、抜去したインプラント情報
4. 手術手技:アプローチ、大転子、最小侵襲手術、ナビゲーションシステム、セメント、セメント商品情報、抗生剤含有セメント、抗生剤情報、骨移植、生体活性材料の使用、生体活性材料商品情報、補強部品、補強部品商品情報
5. 使用したコンポーネント(股臼側、インサート、大腿骨側、骨頭、スクリュー、その他)
② 関節鏡視下手術
1. 手術のプロファイル:術中のトラブル
2. 部位/手術内容:手術部位(膝関節、肘関節、肩関節、手関節、足関節、その他の部位)
3. 膝関節:実施した鏡視下手術(半月板切除術/縫合術、前十字靱帯再建術、後十字靱帯再建術、ACL,PCL 以外の靱帯手術、複合靱帯再建術/修復術、軟骨修復術、滑膜切除術・デブリドマン)
4. 肩関節:実施した鏡視下手術(腱板修復術、バンカート修復術、その他の関節唇手術、HAGL/関節包修復術、観血的関節授動術、デブリドマン、肩峰形成術、再鏡視)
5. 足関節:実施した鏡視下手術(足関節前方インピンジメント症候群に対する鏡視下手術、足関節後方インピンジメント症候群に対する鏡視下手術、骨軟骨損傷に対する鏡視下手術または検査、鏡視下関節固定術、新鮮または陳旧性靱帯損傷に対する鏡視下手術または検査)
6. 股関節:実施した鏡視下手術(股関節インピンジメント、股関節唇処置、臼蓋緑領域のMAHORN 分類、大腿骨頭靱帯、遊離体、臼蓋形成不全の処置)
7. 灌流液:使用した灌流液、灌流液の使用量、灌流方法
8. 術中・術後合併症:手術器具の破損、手術での合併組織損傷、術後合併症
③ 上記以外の手術は順次、関連学会(日本脊椎インストゥルメンテ−ション学会・日本骨折治療学会・日本骨関節感染症学会等)の要望に応じて追加。
3. 利⽤する者の範囲
A) 登録されたデータを利活⽤して医学研究を実施する際には、⽇本整形外科学会が審査の上、⽇本整形外科学会員⼜は関連学会員が利⽤する
B) 有害事象や不具合が発⽣した場合、医学的・⼈道的⾒地から登録されたデータを製造販売業者や審査機関に提供する
C) 療の進歩や安全性向上を⽬的とした医療機器の開発や改良のために製造販売企業に提供する
4. 情報の管理について責任を有する者の⽒名⼜は名称
A) 公益社団法⼈ ⽇本整形外科学会
B) 理事 種市 洋 (症例レジストリー委員会担当)
5. 研究対象者⼜はその代理⼈の求めに応じて、研究対象者が識別される試料・情報の利⽤⼜は他の研究機関への提供を停⽌する。
6. 5.の研究対象者⼜はその代理⼈の求めを受け付ける⽅法
A) 受付先
神鋼記念病院整形外科
〒651-0072 神戸市中央区脇浜町1-4-47
電話 078-261-6711
B) 受付⽅法
窓⼝での受付
郵送 同上
電話 同上
「乳がん微小環境形成に関わる分子生物学的機序の生体資料を用いた探索研究」について
京都大学乳腺外科関連病院で乳がん患者さんの血液検体約7000検体が集まりました。ひとえにご協力いただいた患者さんのおかげです。この約7000検体のうち約2000検体から乳がんに関連する遺伝子を京都大学にて解析しました。遺伝子変異のあった方が当院の検体からも出ています。当初、本研究での開示はしない予定でしたが、現在は乳がん、卵巣がんに関してリスクを下げる検診、予防的治療が可能となり、研究であっても開示希望の方には開示する方向性にむかっています。前述のように、検体を提供していただいた患者さん全員に遺伝子解析は施行されていませんが、施行された患者さんには開示を行って行こうと考えています。遺伝に関する事なので“開示を希望されない患者さん”は主治医までご連絡ください。ご検討宜しくお願いします。
問い合わせ窓口
神鋼記念病院 乳腺センター長 山神 和彦
〒651-0072 神戸市中央区脇浜町1丁目4-47
TEL:078-261-6711(代表)・FAX:078-261-6726
「肺高血圧症患者の四肢骨格筋機能がQOL(生活の質)に与える影響評価」について
患者さんへ
研究課題名
肺高血圧症患者の四肢骨格筋機能がQOL(生活の質)に与える影響評価
はじめに
兵庫県下の肺高血圧診療施設では、2014年4月1日から2024年3月31日の期間中に入院または外来において、肺高血圧症の診断または治療を受けられた患者さんを対象に研究を実施しております。内容については下記のとおりとなっております。
尚、この研究についてご質問等ございましたら、最後に記載しております[問い合わせ窓口]までご連絡ください。
研究の意義および目的
肺高血圧症と診断された患者さんには酸素・利尿剤・肺血管拡張薬・バルーン肺動脈拡張術・外科的肺動脈血栓内膜摘除術などにより治療が行われますが、その効果判定は、右心カテーテル検査や心エコーにより肺高血圧の重症度を測定して評価しております。肺高血圧の重症度はQOL(生活の質)に影響する因子として知られていますが、四肢筋力も肺高血圧の重症者で低下していることが報告され、QOL低下の一因となっていることが予想されます。しかし、四肢筋力低下がどのように患者様のQOLやADL(日常生活動作)に影響しているか依然不明であります。この度、本研究で肺高血圧患者における四肢筋力低下の臨床的意義の検討を行うために、本研究を開始し、今後の肺高血圧治療の発展に貢献したいと考えております。
研究期間
この研究は、2014年4月1日から2024年3月31日までの症例を解析予定です。
取り扱うデータ
患者背景(性別、年齢、身長、体重、使用した薬剤)、血液検査、右心カテーテル検査、心エコー、WHO機能クラス、運動機能(6分間歩行距離、心肺運動負荷検査)、呼吸機能検査、健康関連QOL(生活の質)尺度、ADL(日常生活動作)指標、身体組成・筋力測定値等
個人情報保護の方法
個人情報、検査結果などの記録、保管は第三者が直接患者さんを識別できないよう登録時に定めた登録番号を用いて行います。また得られた記録は、インターネットに接続していない外部記憶装置に記録し、各肺高血圧診療施設の鍵のかかる保管庫に保管します。
研究へのデータ提供による利益・不利益
利益・・・本研究にデータをご提供いただいた患者さん個人には特に利益と考えられるようなことはございません。
不利益・・・通常診療の範囲内で施行するため、特にありません。
研究終了後のデータの取り扱いについて
この研究で取得した患者さんの治療に関する情報は、論文等の発表から10年間は保管され、その後は患者さんを識別する情報を復元不可能な状態にして破棄されます。また、患者さんが本研究に関するデータ使用の取り止めを申出された際、申出の時点で本研究に関わる情報は復元不可能な状態で破棄いたします。
研究成果の公表について
研究成果が学術目的のために論文や学会で公表されることがありますが、その場合も、患者さんの個人情報の秘密は厳重に守られますので、第三者に患者さんの個人情報が明らかになることはありません。
研究へのデータ使用の取り止めについて
いつでも可能です。取りやめを希望されたからといって、何ら不利益を受けることはありませんので、データを本研究に用いられたくない場合には、下記[問い合わせ窓口]までご連絡ください。取り止めの希望を受けた場合、それ以降、患者さんのデータを本研究に用いることはありません。しかしながら、すでに研究成果が論文などで公表されていた場合のように、結果を廃棄できない場合もあります。
研究機関
この研究は以下の研究機関で実施いたします。
代表研究機関:神鋼記念病院 循環器内科 (研究代表者:中山和彦)
協力研究機関:随時追加
問い合わせ窓口
この研究についてのご質問だけでなく、ご自身のデータが本研究に用いられているかどうかをお知りになりたい場合や、ご自身のデータの使用を望まれない場合など、この研究に関することは、どうぞ下記の窓口までお問い合わせ下さい。
代表研究機関
研究代表者:神鋼記念病院 循環器内科 中山 和彦
代表研究機関:神鋼記念病院 循環器内科
住所:〒651-0072 神戸市中央区脇浜町1丁目4-47
TEL:078-261-6711・FAX:078-261-6726
神鋼記念病院脳神経外科にて神経系疾患で入院された方およびそのご家族の方へ
本院は、一般社団法人日本脳神経外科学会(以下、日本脳神経外科学会)が実施するデータベース研究事業に参加しています。この研究は、脳神経外科の患者さんに最善の医療を提供することを目的とする全国的な調査事業です。 この研究の対象者に該当する可能性がある方で、研究への協力を希望されない場合、あるいは協力を途中でおやめになりたい場合は、退院後3カ月以内に末尾に記載の問い合わせ先までご連絡ください。
研究課題
一般社団法人日本脳神経外科学会データベース研究事業(Japan Neurosurgical Database:JND)
研究機関名及び自機関の研究責任者氏名
この研究が行われる研究機関と研究責任者は次に示すとおりです。
研究機関 神鋼記念病院
研究責任者 上野 泰 脳神経外科部長
機関の長 東山 洋 病院長
担当業務 データ提供
共同研究機関
主任研究機関 一般社団法人日本脳神経外科学会
研究代表者 理事長 齊藤延人
担当業務 研究計画立案・データ取得・データ解析
※その他の共同研究機関は、別紙のとおり。
既存情報の提供のみを行う機関
全国の日本脳神経外科学会 専門研修プログラム基幹施設、連携施設、関連施設として登録された脳神経外科施設(およそ1,200施設)、その他脳神経外科専門医の所属する施設(およそ800施設)
業務委託先
(株)ケーアイエス(所在地:〒103-0014 東京都中央区日本橋蛎殻町1-36-7 蛎殻町千葉ビル7階)へ、インターネットを介する症例登録システムおよび高いセキュリティを持つサーバーの保守・管理、および登録されたデータの管理を委託する。
この研究に利用する情報は共同研究機関(及び委託機関)、日本脳神経外科学会の理事会が承認する臨床研究の範囲のみで利用されます。
研究期間
承認日~2028年9月30日
本研究は長期にわたる研究を計画しています。記載の研究期間終了後も継続する場合は、研究期間延長の申請を行う予定です。
対象となる方
2023年10月1日~2028年9月30日の間に当院脳神経外科に入院された方。
研究目的・意義
本研究の目的は、日本脳神経外科学会の会員や専門医が所属する、日本全国の脳神経外科施設における手術を含む医療情報を登録し、集計・分析することで医療の質の向上に役立て、患者さんに最善の医療を提供することを目指すことです。日本の脳神経外科医療の実態を「見える化」し、明らかとなった課題に対して実際のデータに基づく改善策の検討や、施設、地域や全国単位での医療の水準を明らかにし、比較することなどが可能となります。
また分析結果から、より正確に手術や治療にともなう危険が明らかとなり、担当医は患者さんやご家族とともに、治療に伴う危険と利益を共有した上で、治療方針を決定することができます。全国の脳神経外科医療の実態を俯瞰した視点で検証することで、全国の患者さんが安心して手術・治療を受けられるようにするため、より良い脳神経外科専門医制度のあり方を検証するための基礎資料ともなります。
研究の方法
本研究は、日本脳神経外科学会が主導する国内の多施設共同研究であり、当院脳神経外科に入院し、治療や手術を受けられた患者さん全てを対象とさせていただく予定です。本研究は2018年より開始されており、すでに約220万件強の患者さん情報が登録されております。今後、新たに日本全国で年間約60万件の患者さん情報の登録を予定しており、具体的な研究登録項目は以下にお示ししますが、個人を特定される情報は含みません。これまでの診療で診療録(カルテ)に記録されている年齢や入退院日、診療内容、手術の方法などの情報を取得して行う研究です。特に対象となる皆さんに新たにご負担いただくことはありません。
提供いただいた情報は、医師により全国から専用のインターネット登録システムを介して1つのデータベースに集められ、電子データのみで業務委託先と共有し、解析を行います。研究対象者の皆さんのお名前等が、業務委託先や他機関に伝わることはありません。
〔本研究で取得する情報〕
①施設情報
②患者情報
• 生年月(生年月まで必須)
• 年齢
• 性別
• 登録の拒否申請
• 患者居住地の郵便番号(上3桁のみ)
• 発症日
• 発症前mRankin scale
③主治医情報
④入院情報
• 入院年月日
• 入院経路
• 予定入院/緊急入院
• 救急搬送の有無
• 入院時Glasgow Coma Scale(GCS) ※神経外傷のみ
⑤退院情報
• 退院年月日
• 在院日数
• 退院先
• 退院時mRankin Scale
• 退院時Glasgow Outcome Scale (GOS) ※神経外傷のみ
⑥診療目的
• 診断検査
• 教育入院
• 内科治療
• 手術
• 化学療法
• 放射線治療
• リハビリテーション
• 終末期管理
• その他の脳腫瘍補助療法
⑦診断検査
• CT
• MRI
• 脳波
• 核医学
• 高次脳機能検査
• 脊髄造影
• カテーテル血管撮影/読影
• その他
⑧内科治療
• 抗血小板療法
• 抗凝固療法
• 脳保護療法
• 抗浮腫療法
• けいれん てんかん 薬物療法
• 頭痛 薬物療法
• モニタリング下の神経集中治療
• 感染症治療
• その他
⑨化学療法
⑩放射線治療
• 定位放射線治療
• 定位放射線治療以外
⑪手術
大分類 (以下、大分類ごとに、主病名、発症形式、術式を登録)
• 脳血管障害
• 脳腫瘍
• 頭部外傷
• 水頭症/奇形
• 脊髄/脊椎/末梢神経
• 機能的脳神経外科
• 脳症/感染症/炎症性疾患/その他
主病名
発症形式/受傷機転(頭部外傷のみ)/基礎疾患(水頭症/奇形のみ)/病変高位(脊髄/脊椎/末梢神経のみ)
術式
⑫手術情報
• 手術日
• 手術時年齢
• 術式分類
• 術者
• 指導的助手
• 開頭術者
• 助手
• 見学
• 麻酔法
• 手術回数
なお、研究計画書や研究の方法に関する資料を入手・閲覧して、研究内容を詳しくお知りになりたい場合は、末尾の連絡先にお問い合わせください。他の研究対象者の個人情報等の保護や研究の独創性確保に支障がない範囲でご提供させていただきます。
個人情報の保護
この研究に関わって収集される情報は、外部に漏えいすることのないよう、慎重に取り扱う必要があります。
〇個人情報と研究用IDを結びつける(対応表を作成する)場合
取得した情報は、氏名・患者ID等の個人情報を削り、代わりに新しく研究用の符号をつけ、どなたのものか分からないようにします。
どなたのものか分からないように加工した情報は、日本脳神経外科学会と契約した委託先企業が管理するインターネットサーバーに送られ解析・保存されます。
ただし、必要な場合には、当研究室/当診療科においてこの符号を元の氏名等に戻す操作を行うこともできます。
この研究のためにご自分(あるいはご家族)のデータを使用してほしくない場合は主治医にお伝えいただくか、下記の問い合わせ先に退院後、3カ月以内にご連絡ください。研究に参加いただけない場合でも、将来にわたって不利益が生じることはありません。
ご連絡をいただかなかった場合、ご了承いただいたものとさせていただきます。
研究の成果は、あなたの氏名等の個人情報が明らかにならないようにした上で、学会発表や学術雑誌で公表します。
取得した情報は厳重な管理のもと、研究期間終了(論文発表後)10年間保存されます。保管期間終了後には、データ記録媒体から復元できない形で削除することで廃棄します。なお研究データを統計データとしてまとめたものについてはお問い合わせがあれば開示いたしますので下記までご連絡ください。
また、これらの情報は保管期間中に、この研究以外の研究に使用される可能性もあります。その場合には改めて倫理委員会の承認を受け、あなたの同意を得るか、または情報公開により研究対象者となることを拒否する機会を設けます。研究の詳細情報は、日本脳神経外科学会ホームページ>一般の方へ>研究情報の公開について(https://jns-official.jp/public/studyinfo)に掲載いたします。
尚、提供いただいた試料・情報の管理の責任者は下記の通りです。
試料・情報の管理責任者
所属:神鋼記念病院
氏名:研究責任者
この研究は、東京大学医学部倫理委員会の承認を受け、院長 東山 洋 の許可を受けて実施するものです。
この研究に関する費用は、日本脳神経外科学会の事業費から支出されています。
本研究に関して、開示すべき利益相反関係はありません。
尚、あなたへの謝金はございません。
この研究について、わからないことや聞きたいこと、何か心配なことがありましたら、お気軽に下記の連絡先までお問い合わせください。
【連絡・お問い合わせ先】
研究責任者:上野 泰
連絡担当者:上野 泰
〒651-0072兵庫県神戸市中央区脇浜町1-4-47
神鋼記念病院
Tel: 078-261-6711 Fax: 078-261-6767
主任研究機関 一般社団法人日本脳神経外科学会
研究代表者 理事長 齊藤 延人
〒113-0033 東京都文京区本郷5-25-16 石川ビル4階
Tel: 03-3812-6226 Fax: 03-3812-2090
e-mail: jns@jnss.or.jp
乳がん微小環境形成に関わる分子生物学的機序の生体資料を用いた探索研究
神鋼記念病院乳腺科に入院または通院中の患者さんへ
研究の目的
乳がんという病気は本来の秩序を破って異常に増殖する細胞(がん細胞)が母乳をつくるための乳腺のなかにできる病気です。従来、がん細胞は自分勝手に増殖しているものと考えられていました。しかし、最近の研究では、がん細胞が発生したり、増えて広がっていくためにはそれだけでは不十分で、 周りを取り囲んでいる細胞や血液(まとめて“微小環境”といいます)の助けが必要なことがわかってきました。この研究の目的は“微小環境”がどのようなしくみでがん細胞を助けているのかを、乳がん患者さんの組織や体液(血液、尿)を最先端の技術を用いて解析し、明らかにすることを目的としています。
研究についての詳細はこちらから
研究方法
乳がんと診断された20歳以上の患者さんにご参加いただきます。現在、診療時に必要な採血時に合せて、血液を10-15ml余分に採取します。ご提供いただいた検体を、特殊な機器を用いて観察したり、がん細胞やがん細胞の周りにいる細胞を分離したりしてその特性や機能をバイオテクノロジーの技術を用いて調べます。患者さんの個人情報は匿名化し、第三者が個人を特定することができないように適切に保護されています。
測定結果のご報告
ご提供いただいた検体を用いて、「がん」のしくみについてさまざまな検討を行います。当研究の結果は検体を提供していただいた患者さん自身の健康や診療に役立つものではありません。このため、測定結果について、直接ご本人にご報告する予定はありません。
この研究によって期待されること
この研究の成果は将来乳がんの診療、治療法の開発にいかされ、乳がん診療の発展に貢献します。
同意の撤回
この研究への参加は、いつでも患者さんの希望によって取りやめることができます。同意の撤回を希望された場合は、遠慮なく担当医師にご相談ください。
費用・利益
この研究で行う検体の分析について、患者さんに費用を負担していただくことはありません。すべて公的研究費等でまかなわれます。
主研究機関
◇主研究者:京都大学医学部附属病院 乳腺外科 教授 戸井 雅和
◇当院における研究責任者:神鋼記念病院 乳腺センター長 山神 和彦
当院における連絡先
神鋼記念病院 乳腺センター
〒651-0072 神戸市中央区脇浜町1丁目4-47
TEL:078-261-6711 ・ FAX:078-261-6726
「乳房良悪性病変のgadobutrol* 造影MRI画像における
画像的特徴に関する検討」について
神鋼記念病院乳腺科で入院あるいは外来診療を受けられた患者さんへ
実施する臨床研究
当院では、乳腺疾患のMRI画像診断に関する臨床研究を実施しております。この研究は「観察研究」と呼ばれるもので、通常の診療で得られた記録をまとめることによって行います。 以下の点をご理解いただき、ご協力いただきますようお願い申し上げます。
*gadobutrolは当院でも使用されているMRI用造影剤の一般名です(商品名ガドビスト)。
この研究の意義、目的、および方法
日本国内の多数の施設から様々な乳腺疾患の情報が収集されるので、乳腺疾患のMRI画像を網羅的に分析することができMRI画像診断の診断能の改善に寄与するものと考えられます。
この研究による医学上の貢献と予測
日本国内の多数の施設から様々な乳腺疾患の情報が収集されるので、乳腺疾患のMRI画像を網羅的に分析することができMRI画像診断の診断能の改善に寄与するものと考えられます。
この研究による患者さんの不利益および危険性
患者さんの診療情報を分析する研究であり、プライバシーも厳重に保護されますので、患者さんに不利益や危険性はありません。
費用や追加の検査
通常の保険診療による画像診断情報と臨床情報の収集と分析ですので、患者さんに余分な費用を負担してもらうことはありません。また、検査方法の変更や追加検査もありません。
個人情報の保護
この研究で得た情報は厳重に管理され、学術目的のみで利用されます。 研究結果は主として統計として処理・解析され発表されるため、個人を特定できることはありません。研究結果の発表に際して、一部の患者さんの画像が参考所見として呈示される可能性がありますが、画像は匿名化されていますので、個人を特定できることはありません。本研究参加者以外の第三者に流出することもありません。以上のように、患者さんのプライバシーは厳重に保護されますのでご安心ください。
ご協力の拒否について
この研究にご自分のデータが使用されることを拒否される場合は、担当医もしくは下記の問い合わせ先に連絡下さい。たとえ、協力を拒否されても、今後の診療の不利益になることはありません。しかし、拒否のお申し出のあった時点で、既に研究結果が論文などで公表されていた場合には、 研究結果を破棄できないことがあります。この場合でも個人が特定されることはありませんので個人情報は保護されます。
研究責任者
東京医科歯科大学医学部 附属病院医療情報部 久保田 一徳
※神鋼記念病院は分担研究施設です
神鋼記念病院(分担研究施設)における研究組織
◇放射線センター:門澤 秀一(当院代表研究者)
◇乳腺センター :山神 和彦
当院における連絡先
神鋼記念病院 放射線センター:門澤 秀一
〒651-0072 神戸市中央区脇浜町1丁目4-47
TEL:078-261-6711 ・ FAX:078-261-6726